Militantní aktivisté jsou vynalézaví a mocní. I nám v Evropě lobistická anti-GMO fronta u rostlin ukázala, zač je toho loket. Americká FDA dostala nedávno na stůl požadavek ohledně léčby molekulárně genetickými metodami, při níž se má vylepšovat lidský genom. Možná stojí za porovnání, jak se k problému genetických modifikací staví úřad tady a tam. Pravdou je, že bruselští legislativci to měli s povolováním genových modifikací složitější. Nemohli svým verdiktem nezesměšnit politická rozhodnutí svých lídrů a současně dát za pravdu vědeckým autoritám. Vlastně ani neměli jinou možnost, než desetiletí si hrát na mrtvého brouka. V jedné z takových kauz s lidskými buňkami, si svou Bruselskou anabázi užil i Britský patentový úřad. Letitý spor museli řešit až lucenburští talárníci. A jak jsme v článku Velký spor o malých buňkách psali, stejně to nakonec zahráli do autu. Až se jeden přestává divit, že se teď za kanálem nyní rozhodli, jak se rozhodli.
Nejvyšší americká instituce nejspíš nechce přispět k podobnému parcelování Spojených států a tak řeší požadavek na změnu dědičné informace pomocí CRISPR rychle a do jasného verdiktu a ten může být jen ano, nebo ne.
Je pravdou, že o nápravu porouchaných genů, o něž nyní v této kauze jde, se v několika zemích již dříve vědci pokoušeli. A že se jim to do jisté míry také podařilo. V několika málo případech pokusně i na lidech. Jenže to všechno zatím vždy byly akce, při nichž u nápravy funkce poškozeného genu muselo asistovat štěstí. Vnášený úsek DNA se pacientovi zabudovával do genomu tam, kam se mu zrovna zamanulo. Náš autor Jaroslav Petr, to kdysi přirovnal k situaci, jako když si přijedete do servisu nechat opravit rozbité světlo a automechanik vám namontoval nové. Pokud jste měli štěstí, připevnil ho do míst, odkud se s ním dalo svítit dopředu a s tím správným sklonem. Ještě před třemi lety jsme neuměli „havarovaný“ gen v dědičné informaci buněk nahradit jiným genem neporušeným v jeho původním „pelíšku“. Poškozený gen se ponechával svému osudu, a navíc jsme do organismu vkládali funkční gen, takříkajíc přetlakem v nadbytku. Kontrolu nad tím, kam se vkládané geny „vmáčknou“, jsme neměli žádnou. Stávalo se, že se nainstalovaly někam, kde pošramotily jiné funkce dědičné informace. Tak se to stalo francouzskému týmu, který léčil dítka postižená nedostatečností imunitního systému. Vědci jim nefunkční systém zprovoznili, ale časem se ukázalo, že se geny u třech z dvanácti robátek, zabudovaly na nevhodná místa a u těch pak po nějaké době, propukla leukemie. Tomu by ale nyní technika CRISPR měla udělat přítrž.

Co je CRISPR?
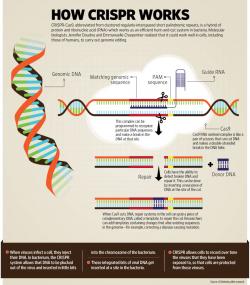
Nejnovější a zároveň nejmocnější nástroj ke stříhání a úpravu genomu. Správně celým názvem je CRISPR-Cas9. Novináři odkoukali od výzkumníků laboratorní žargon a začali psát jen „CRISPR“, což už se prakticky všeobecně ujalo. Je ale dobré mít na paměti, že to bez Cas9 nefunguje a že podstatou je obranný systém bakterií. Něco jako jejich očkovací průkaz. Bakterie si do něj zapisuje s jakým virem se již setkala. Nepřítele si totiž s pomocí CRISPR rozstříhá a pak jeho části vloží do svého genomu, jako do deníčku. Informaci pro strýčka příhodu případného dalšího setkání, kdy už by bakterie na infekci zareagovala pohotověji. Taže CRISPR toho znamená poměrně dost, podle toho z jakého úhlu se na jeho funkci ptáme. Je to opakující se sekvence nukleotidů ( původně vyplňující virální DNA). CRISPR je také lokus, tedy místo na chromozomu bakterie. Z pohledu funkce to je rozpoznávací systém virové DNA, který nepřítele umí rozstříhat a začlenit do svého genomu v místech zvaných CRISPR lokus. Cas9 je úsek DNA, který kóduje proteiny, spolupracuje s CRISPRem a vzniklé proteiny (helikázy a nukleázy) jsou instrumenty, které dokážou rozplétat a „stříhat“ DNA. Popsané bakteriální nářadí se dá využít jako technika k cílené manipulaci s genomem. Jako první na to upozornily dvě vědkyně a to nezávisle na sobě - Jennifer Doudna z University of California v Berkeley a Emmanuelle Charpentier, původem Francouzska. Podle nich je to prý jednoduché. Stačí vzít enzym, kterému se říká nůžky na stříhání DNA, doplnit jej o kousky, které pouhým přiložením poznají, kdy jsou na tom správném místě a kde se má stříhat a to je vše. Tím geniálním naváděcím systémem je krátký řetězec ribonukleové kyseliny. On rozhodne o místu, kde enzym nukleáza provede svůj střih. Protože lidský genom už máme přečtený celý, není problém narušit v něm kterékoliv místo, které si zamaneme. A nejen to. Pak do toho místa můžeme stejným náčiním také vnést úsek cizí, nebo vlastní opravené DNA. Tím nejjednodušším a na myších ověřeným způsobem, se vylepšení genomu pacienta provádí pomocí „záplaty“. Do těl nemocných buněk se aplikuje CRISPR-Cas, zacílený na mutací poškozený gen. Zároveň se do nich vpraví na poškozený gen krátký úsek DNA se správnou (opravenou) sekvencí. Buňky už jsou od přírody takové, že poškozený gen se snaží rychle zalátat vším, co mají po ruce a tak do díry, zhruba v jednom ze dvou set případů, místo zalepí podsunutou záplatou. Tím, jak se buňky množí, a těm opraveným se to daří radostněji, roste v pacientovi i počet opravených, nebo chcete-li zdravých, buněk. Jak pokus s myšmi v případě léčby poruchy zvané tyrosinémie ukázal, zdravých buněk nakonec měly pacientky v těle zhruba jednu třetinu. To stačilo aby se hlodavcům začalo dařit odstraňovat z těla toxické látky poškozující ledviny, játra i mozek, průvodní zdravotní problémy byly zažehnány a choutky s radostí do života se jim vrátily.

Federální porota, kterou si před časem americká FDA k posouzení studie v níž se bude nemocným odebírat z krve jeden typ bílých krvinek (T buňky) a po jejich úpravě zase vracet zpět, dala již k takové léčbě souhlasné dobrozdání (National Institutes of Health’s Recombinant DNA Advisory Committee). K zahájení léčby jsou sice ještě potřeba dvě věci, ale ty už jsou jen otázkou krátkého času. Souhlas NIH pod něž zdravotnická zařízení, kde se léčba bude realizovat spadají. A prakticky jen formálního souhlasného vyjádření úřadu (FDA). Kliniky, kde se léčba bude provádět, už jsou také známy. Jednou má být zařízení University of Pennsylvania. Další pak biotechnologická společnost Editas. Finančně akci zajišťuje Sean Parker a sice prostřednictvím svého soukromého výzkumného ústavu. Není to ústav na jaký jsme u nás zvyklí. Nejde o jednu budovu, ale šest center, které jsou „přifařeny“ k institucím, které v základním výzkumu imunulogie hodně znamenají: Memorial Sloan Kettering Cancer Center, Stanford University, University of California, Los Angeles, University of California, San Francisco, University of Pennsylvania, a the University of Texas MD Anderson Cancer Center. Ústav má čtyřicet laboratoří a v nich 300 špičkových vědců tahajících za jeden provaz. Tím je imunologický boj s rakovinou.
Lepší odborníky k tomu asi už vybrat ani nešlo a tak v brzké době, odpůrcům genetického vylepšování člověka navzdory, dojde u řady nemocných k úpravám genů imunitního systému. Dvěma vnesenými geny poučené T buňky by měly vést boj s rakovinou zvrhlými kolegyněmi - původkyním myelomu, sarkomu a melanomu. Společnost Editas hodlá přisět léčbou některých typů slepoty.
Schvalovací proces by neměl narazit na odpor, protože editace pacientových genů se dotkne jen specifické části buněk. Takovým úpravám se říká somatické. Nyní zvažované vylepšování člověka se tedy zatím netýkají změn v buňkách embryí, vajíček ani spermií (zárodečné genové terapie) a opravy se proto nebudou přenášet na potomstvo léčených osob.
Možná si vzpomenete na novinové titulky z letošního ledna, jak se v EU začnou geneticky modifikovat lidská embrya. Mohli bychom snadno nabýt dojmu, jak jsme už strýčka Sama dostihli a předběhli. Jenže to, k čemu Britům udělil souhlas jejich zdravotnický úřad HFEA (Úřad pro početí a embryologii) a co tak silně popudilo zbytek neanglikánské křesťanské EU, je jen uplatnění techniky CRISPR na lidská embrya v prvních sedmi dnech po oplodnění. Má to ale háček. Je tam podmínka, že je nesmějí implantovat. Což v překladu do normální mluvy znamená, že musejí být zničena. Takže pro praxi a k léčbě, zatím nic.
Ono na tom ale zase tak moc nezáleží, kde se CRISPR(em) začnou lidé léčit jako první, hlavně aby už to bylo, protože pro mnohé to je jediná naděje. Nemusí přitom jít drahou léčbu, jako v případě zde již zmíněného záplatování. I pouhé ničení DNA v tom správném místě může zachraňovat životy. Nádorové buňky, které se rozhodly nekontrolovaně se množit, si k obrazu svému musely upravit naše geny. Střih CRISPRem právě v těchto upravených genech, má šanci zvrhlým buňkám jejich choutky na množení, znechutit. Laicky řečeno, léčit lze i pouhým děláním děr.
Nová technika CRISPR posunula opravu genomů na zcela jinou úroveň a leukemie, která postihla některé pacienty francouzského týmu, v oněch pionýrských dobách genového inženýrství a snah o nápravu chyb přírody, již novou technikou léčeným, nehrozí. Bylo by škodou, kdyby ti, co se rádi schovávají za etiku, dál vše zdržovali. Často totiž jde z jejich strany jen o obhajování své židle a úřadu. Rozdíl mezi vlastním a cizím, na co tak rádi při svém strašení kladou důraz, se už dávno začal stírat. Gen je jen sekvence bází (kousek DNA) a návod pro buňku k nějaké činnosti. Zatímco pro genetiky je mutantem ten, komu mutace gen poničila, pro anti-GMO aktivisty je mutantem organismus s vneseným genem a jedno o jaký gen jde. Z jejich pohledu jde hlavně „o princip“.
I když stávající souhlas k provádění genetických modifikací a vylepšování rodu Homo, nemá se změnou genomu budoucích generací zatím nic společného, přesto je označován za: „Malý krok pro několik málo pacientů, ale velký skok pro lidstvo“. Slova tentokrát mají ale poněkud jiný význam, než jaký měla v době, kdy je pronášel Neil Amstrong. Tehdy znamenala pokrok ve smyslu vědeckého pokroku. Dnes se tím myslí vnímání genetických modifikací veřejností. Ta je odpůrci modifikací tak zmatená, že opravu genů a často i jen pouhou jejich konzumaci, vnímá jako něco, co je proti přírodě a Bohu. Projekt, který dostává v těchto dnech zelenou, už ani američtí zelení nemají šanci zakázat argumentacemi o předběžné opatrnosti. Léčba technologií CRISPR má všechny šance v uzdravování lidí uspět. Nemusí totiž jít jen o opravu genomu lidí, ale třeba o to, čemu se začíná říkat crisprová antibiotika. Paradoxně o nějaké nové antibiotikum vlastně ani nejde a ani o jejich vylepšování. Nejspíš ten název vznikl proto, aby technika měnící genom mikrobů a dělající z nich GMO, ušla zájmu těch, co si rádi oblékají bílé pláště s plynovými maskami a pak demonstrativně chodí ničit políčka a podpalovat laboratoře.
Jak všichni víme, prevíty jako třeba MRSA, si můžeme z nemocnice domů přinést i když jsme tam šli třeba jen odstranit si bradavici na nose, nebo navštívit příbuzného. Nemocnice jsou totiž ideálním místem pro vznik i šíření reizistentních bakteriálních kmenů. Právě rezistence nás připravila o většinu ještě nedávno vysoce účinných antibiotik. Souvisí to s geny, které si bakterie předávají a kterými se naučí molekuly antibiotika štěpit, nebo je ze svých těl vylučovat. Ať už je jejich obranný mechanismus jakýkoliv, je vždy spojen s konkrétním genem. S objevem techniky CRISPR se nám otevřela možnost vyřazovat jim je ze hry.
Pokusy se stafylokokem obdařeným genem pro rezistenci na antibiotikum methicilin, poté, co mu technikou SRISPR do jeho genu rezistence střihli, už nebyl dál MRSA (česky „zlatý stafylokok“), ale byl z něj zase jen „stříbrný stafylokok“ s nímž si poradil i starý dobrý penicilin.
Široké pole působnosti, které technika CRISPR jako genomového editoru, medicíně otevírá, spolu s rostoucím počtem „modifikovaných uzdravených“, by mohly přispět ke změně názorů na uplatňování GMO i v dalších oblastech. Informovaná společnost by měla přestat politiky svádět k tanečkům s vyhlašováním nesmyslných zákazů, které jsou výsledkem prostého kalkulu volebních preferencí.
Amerika svým povolením genového vylepšování lidí nabírá kurz asijského zdravotnictví s pragmatickým vztahem ke genovým modifikacím. Nejspíš ji k tom donutila rozmáhající se transplantační turistika jejich občanů za léčbou kmenovými buňkami. U nás v Česku jsme směr také odhadli dobře, jen jsme malinko popletli tu koncovku. Místo přebírání výsledků z molekulární genetiky, importujeme alternativní přípravky a ideje založené na léčbě mumiem, tygřími kostmi, práškem z „draků“ (zkamenělin) a bylinek s rohem nosorožce.
Literatura
MIT Technology Review, FDA, NIH, Popular Science,Washington Post, Biospace