Všechny rakoviny krve zvané leukemie mají co do činění s poruchou regulace množení bílých krvinek. Krvetvorné buňky jakoby ztratily soudnost a aniž by patřičně vyzrály, začnou se o překot dělit. Stanou se z nich paraziti, kteří tělu užitek nepřinášejí, jen jako nenasytné vyžírky spotřebovávají všechny dostupné živiny. Právě jejich metabolismu jedoucího na plný plyn využívá chemoterapie. Nabízí vyvíjejícím se krvinkám jed, nebo radioaktivní látku s krátkým poločasem rozpadu v podobě substrátu, který buňky ke svému růstu potřebují. Chemoterapie spoléhá na to, že nejrychleji po živinách sáhnou hladové rakovinné buňky a cílem je zajistit v těle nemocného takový stav, v němž všechny ty rychle rostoucí, obdrží letální dávku a ty normální jen takovou, ze které jsou schopny se zmátožit. Přes veškerou snahu se léčba občas nevyvede a pacientovi se nemoc vrací. Na to proč, je celá řada názorů. Dva z nich se zdají být nejpravděpodobnější. První viní z neúspěchu špatný odhad množství aplikovaného jedu, takže se nedostalo na všechny zvrhlé buňky. Zvláště ty, které se skrývaly někde, kam účinná látka v dostatečném množství nepronikla, například proto, že ji vychytaly zdravé buňky v okolí, i ty se potřebují živit, zvláště když zrovna plní nějaký náročnější úkol.
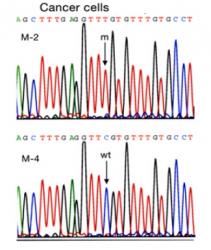
Druhý z názorů předpokládá, že část rakovinných buněk nejede na maximum a že si ve svém dělení dávají na čas. Z hlediska apetitu se pak tyto zvrhlé loudalky jeví stejně, jako zdravé buňky našeho těla.
Proč vědce zajímá, která z variant je ta správná?
Proto, že na tom záleží způsob léčby. V prvním případě by největší úspěch zaručovalo jakési balancování na ostří nože s co největšími dávkami jedů aby došlo k nasycení všech žravých buněk. Má to sice také svůj háček - čím vyšší dávka chemoterapeutika, tím větší poškození i těch, které k životu potřebujeme a hranice mezi životem a smrtí se tak stává velmi úzkou. I tak má ale nemocný velkou šanci, že ho klasická chemoterapie uzdraví.
V případě správnosti druhé varianty, kdy se mezi rakovinými buňkami vyskytují i ty pomalu se množící, je přílišné riskování zbytečné. Chovají se tak trochu jakoby dbaly na svou linii a ani ten nejprostřenější stůl s nejvybranějšími jedovými chody je neláká. Vědci je označili termínem „CSC“, což je zkratka z anglického cancer stem cells, neboli kmenové rakovinné buňky. Ty se nemusí skrývat někde na periferii, kam se k nim léčebná „krmě“ nedostane. Producírují se nám okolo nabízených "lahůdek“, aniž by podlehly pokušení se jimi přecpat. Proto léčbu přežijí a mohou později dávat vznik těm agilnějším rakovinovým otesánkům, kteří se již množí hlava nehlava.

Tým Ehuda Shapira z Weizmannova ústavu, spolu s lékaři z Rambamova Lékařského Centra a Technionu v Haifě, se pokusil přijít věci na kloub. Izraelci zvolili cestu rekonstrukce genealogického stromu života rakovinových buněk. Sestavovali něco podobného, jako když si někdo skládá rodokmen předků. Jen místo zápisů z matrik se řídili mutacemi. I ty jsou zapsány v buněčné DNA. Ve zdravých buňkách, stejně jako v těch nemocných, vznikají náhodné mutace. Říká se jim neutrální somatické mutace. Mnohé jsou jedinečné a v buňkách jiných tkání se nevyskytují. Jak se postupně tyto změny v jaderné DNA vrší, lze podle nich sestavit „strom života“. Z něho je pak patrné, která buňka z které tkáně vznikla a kdy k tomu přibližně došlo. Vše se děje podle zásady, že dceřinné buňky mají více mutací, než jejich buňka mateřská.
Problém je v tom, že genom je obrovský a mutace v něm poměrně zřídkavé. Jejich hledání je příslovečným pátráním po jehle v kupce sena se všemi necnostmi vysokých nákladů a zdlouhavosti takového vyšetření. Vědce napadlo využít těch míst v genomu, kde dochází k mutacím častěji. Nejde tedy o záležitost té části DNA v níž jsou geny, ale úseků, kterým se říká satelity. Autoři našli v DNA sto takových oblastí v nichž se mutace vyskytují až tisíkrát častěji, než v jiných částech genomu. Protože nic nezpůsobují, tak nás většinou nezajímají. K určení původu buněk jsou ale požehnáním. Není třeba testovat celou dlouhou molekulu DNA, ale stačí k tomu jen přečíst krátké úseky. Nejen, že vyšetření je rychlé, ale lze udělat i na jednotlivých buňkách.
Izraelským vědcům k rekonstrukci původu linie leukemických buněk stačilo porovnat dva krevní odběry. Toho, který provedli pacientům v čase, kdy u nich leukemii diagnostikovali, s tím, který provedli když se rakovina vrátila. Z mutačních vzorů změn v DNA pak vystopovali původ nově vznikajících rakovinných buněk. Vyšlo jim, že některým z pacientů se po chemoterapii rakovina nevrací jen z buněk, které se jim v těle překotně množí, ale také těch „rozvážných“, které se dělí pomalu. To není dobré zjištění, protože na některé leukemie bude i agresivní a dobře provedená chemoterapie vždy krátká. Na druhé straně jsme o další krůček ve skládání rakovinového puzzle dál. Na některé typy leukemie je třeba hledat jinou, než konvenční strategii léčby. Takovou, která si kromě těch dobře viditelných nepřátelských buněk začne všímat i těch nevýrazných kmenových rakovinových buněk. Alespoň teď už víme, co je třeba hledat - specifické znaky CSC buněk, jimž se nástrahám chemoterapie daří unikat proto, že se svým chováním od těch normálních neliší. Pokud se na těchto buňkách podaří najít nějakou specifickou povrchovou strukturu (výběžek), proti níž by se dala připravit protilátka, pak by už jen stačilo k protilátce schopné vyhledávat svůj cíl, připevnit balíček se smrtící zásilkou. Pokud by tento uměle sestavený atentátník moc neprovokoval náš imunitní systém aby mu dovolil nerušeně kolovat v krvi...
Prameny: Weizmann Institute of Science, Blood