Angela M. Belcherová zasvětila svou vědeckou kariéru virům označovaným stručně M13. Jsou to bakteriofágy, což znamená že napadají bakterie, konkrétně téměř všudypřítomnou Escherichii coli (E. coli). Belcherová ale nezkoumá patogenitu viru M13. S dnes již bývalým kolegou Seung-Wuk Leem v roce 2002 vyvinuli metodu, jak tento mikroorganismus po cílených genetických modifikacích využít pro rozmanité, pro laika překvapivé aplikace. Oba tehdy pracovali na Texaské universitě v Austinu.
O některých výsledcích týmu Belcherové jsme již na Oslu psali, a to je také důkazem, že kromě výzkumu mají američtí vědci promyšlenou i jeho propagaci: Virové baterie, Zavírené batérie, Fágy šikovnými pomocníky při výrobě solárních článků, Fotolýzu vody usnadňuje virus.
V současnosti je Belcherová profesorkou v oboru materiálového výzkumu a bioinženýrství na Massachusettském technickém institutu MIT. Nadále se věnuje aplikacím viru M13 v elektronice.

Její bývalý kolega Lee vytvořil tým v jiné známé vědecké instituci - Kalifornské universitě v Berkeley. Právě jeho skupině vyšel v nejnovějším čísle časopisu Nature článek o dalším zajímavém využití bakteriofágu. Vědci ho přinutili se velice systematicky ukládat na povrch připraveného substrátu a vytvářet tak supramolekulární struktury (s nekovalentními vazbami mezi molekulami) napodobující biologické materiály.
„Nechali jsme se inspirovat přírodou,“ říká Lee. „Ta má jedinečnou schopnost vytvářet složité funkční materiály z jednoduchých stavebních prvků. Objevili jsme způsob jak napodobit tvorbu rozmanitých komplexních přírodních struktur z makromolekul šroubovitého tvaru, jako jsou kolagen, chitin a celulóza, což jsou základní stavební cihličky pro široké spektrum živočišných i rostlinných tkání.“
Při pokusech napodobit přírodní procesy se vědci dostávají do problémů. Ani vyspělé laboratorní zařízení neumožňuje podřídit se požadavkům pro velkou citlivost na všechny působící faktory, které ovlivňují tvorbu biologických struktur v živých organismech. Zůstává tajemstvím, jak příroda zvládá tak přesné řízení.
Elegantní řešení, jak se alespoň trochu přiblížit evolucí vytříbeným výrobním postupům, nabízí právě fág M13, kterého lze použít jako základní stavební jednotku podobně, jakou představuje kolagen v různých tkáních. Pro člověka je tento virus absolutně neškodný, a protože jeho životní cyklus může probíhat jenom uvnitř hostitelské bakteriální buňky, je ve vnějším prostředí stabilní. Má ale i další zajímavé vlastnosti. Povrch jeho "těla" připomínajícího mikrovlákno dlouhé necelou deseti tisícinu milimetru, tvoří 2 700 spirálovitě uspořádaných molekul stejné bílkoviny (p8). Genetickými manipulacemi, tedy umělými zásahy do posloupnosti nukleotidů v genu, jenž je programem pro syntézu tohoto proteinu, lze změnit jeho afinitu k různým látkám, které z prostředí na sebe váže. Virus se jimi pak sám obalí, nebo pokud jsou součástí nějakého povrchu, se na ně „nalepí“. Povětšinou se do genu pro p8 vkládá DNA program pro vhodný peptid (lineární řetězec aminokyselin kratší než u bílkoviny).
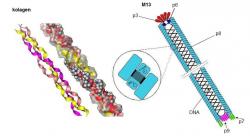
Ještě jednu výhodu povrchová struktura bakteriofágu M13 nabízí. Na koncích vlákna se nacházejí další 4 druhy bílkovin. Na jednom konci mají označení p3 a p6, na tom druhém p7 a p9. Ty lze také geneticky pozměnit, aby se připojovaly k molekulám konkrétních látek. Když takové jsou součástí nějakého povrchu, viry se na nich pomocí elektrostatických sil zachytí a tak se vlastně sami na podkladu uspořádají. Koncovými proteiny se připnou na místa, kde naleznou pro ně „přítažlivé“ molekuly. Samozřejmě vůbec nemusí jít o biologické nebo organické látky, ale například to mohou být i atomy kovů nebo molekuly anorganických sloučenin. Zároveň je možné dosáhnout, aby se vlákna upravených virů připojovala jedním koncem a vytvářela na cílovém povrchu „koberec“, nebo oběma konci, anebo k němu přilnula celým povrchem.
To vše nabízí široké spektrum variací využití M13 jako samoorganizujícího se nano-nosiče různých molekul, který se sám uspořádává do rozmanitých struktur v závislosti od vnějších podmínek.
Tým Seung-Wuk Leeho vytvořil zařízení, které do slaného roztoku s obsahem bakteriofágů M13 kolmo ponořilo tenkou skleněnou deštičku a pak ji velmi pomalu, po setinách milimetru za minutu, vytahovalo. Přitom na linii kontaktu sklo – kapalina docházelo k systematickému samovolnému usazování tenkého filmu z virových vláken (viz video). Výsledný vzor nebyl chaotický, ale překvapivě pravidelný, přičemž jeho struktura závisela od působících faktorů – od koncentrace bakteriofágů v roztoku, jeho viskozity a povrchového napětí, míry odparu na kontaktu se sklem a na rychlosti vytahování destičky. Přitom bylo možné zvolit hodnotu v rozmezí od 10 do 100 mikrometrů za minutu.
Video: Viskozita roztoku, koncentrace virů, míra odparu a rychlost vytahování destičky jsou hlavními faktory, které určují, jaký povrchový vzor vlákna M13 vytvoří. Kredit: Video by Woo-Jae Chung, UC Berkeley
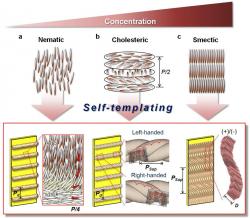
Regulací podmínek vědci získali tři typy vzorů povrchové vrstvy:
a/ Při koncentraci 0,1 až 0, 2 miligramů virových částic na mililitr slaného roztoku se tvořily pravidelné pásy s vlákny uspořádanými střídavě rovnoběžně a kolmo na směr pohybu substrátu. Tedy uložení vláken ve dvou navzájem sousedících pásech bylo navzájem kolmé. U tohoto vzoru bylo možné dosáhnout výrazné trojrozměrné plasticity.
b/ Střední koncentrace (0,25 až 0,5 mg M13 na 1 ml) a rychlost vytahování substrátu 10 až 20 mikrometrů za minutu vedly ke struktuře připomínající vedle sebe uložené zkroucené provázky rovnoběžné s hladinou roztoku. Protože se samouspořádání virových vláken šířilo z okrajové části směrem do středu, z levé strany se tahaly pravotočivé „šňůry“ a z pravé levotočivé.
c/ Při nejvyšší koncentraci v rozsahu 4 až 6 mg/ml vznikala třetí struktura, která připomínala japonské „ramen“ nudle, případně klasický šikmý parketový vzor. Tím na povrchu substrátu vznikaly souběžné vlnovky vinoucí se nahoru, ve směru vytahování z roztoku.

Vědci zjistili, že když jako podklad pro tuto třetí, vysoce organizovanou strukturu použijí namísto skleněné destičky křemennou potaženou zlatým filmem a pokryjí ji třetím typem virové vrstvy, výsledný povrch dokáže rozptylovat světlo způsobem, který doposud nebyl v přírodě ani mezi uměle vyrobenými materiály pozorován. Jeho optické vlastnosti lze ovlivňovat pomocí změn hustoty zachycených vláken M13 (vlnovek). Tato hustota se zvyšuje s poklesem rychlosti vytahování substrátu z roztoku.
„Jemným dolaďováním faktorů, které působí na kinetiku a termodynamiku procesu samoorganizace, dokážeme předem stanovit typ vznikající struktury. Sme schopni řídit míru jeho uspořádání, směr stáčení vláken, jako i šířku, tloušťku a rozestupy ve vzoru výsledné vrstvy,“ vysvětluje postdoktorand Woo-Jae Chung, který je prvním autorem publikace v Nature.
Vědci, aby prokázali biomedicínský potenciál využití virových vrstev, fága M13 geneticky upravili tak, aby na svém povrchu tvořil peptidy ovlivňující růst tkání. Pak využili povrchovou strukturu z jeho vláken jako kostru, v níž se z roztoku usazoval fosforečnan vápenatý a vytvářel materiál velmi podobný zubní sklovině.
Množení i geneticky upravených fágů pomocí hostitelských buněk E. coli je jednoduché a rychlé. I „výroba“ virové povrchové vrstvy běží samostatně, stačí nastavit podmínky. To vše nahrává možnému praktickému využití. Jenže za téměř deset uplynulých let bylo publikováno několik článků s výsledky různých studií využívajících M13 jako samoorganizující se stavební prvek, který se dokáže sám navázat na podklad a jehož povrchová bílkovina může odchytávat z prostředí specifické látky, obalovat jimi celé vlákno bakteriofágu a tím ho přetvořit na zajímavou nanostrukturu (například elektrodu minibaterie). Přesto se z pokusů zatím nezrodila žádná reálně používaná aplikace. To tak trochu tlumí fantazii při vymýšlení, kde se s novými „zavirovanými“ povrchy v budoucnu setkáme.
Poznámka: Pro lepší pochopení struktur nových povrchových vrstev doporučujeme si prohlédnout zajímavé obrázky a grafy ve volně dostupných doplňkových informacích.
Zdroj: UC Berkeley News, Nature