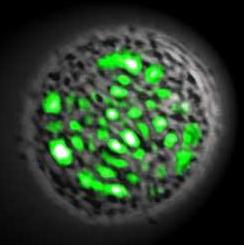
Fluorescenční protein zviditelňuje neviditelné
Před téměř 40 lety, v roce 1962, se podařilo tříčlennému týmu Osamu Shimomury ze světélkující medúzy druhu Aequorea victoria extrahovat zelený fluorescenční protein a popsat jeho vlastnosti. V roce 2008 byl Osamu Shimomura součástí jiného vědeckého trojlístku, který byl oceněn Nobelovou cenou za chemii. Fluorescenční proteiny, jejichž krátký genetický kód lze poměrně jednoduše vpravit do živé buňky, se za ty čtyři desetiletí staly pro současnou biologii a genetiku nenahraditelnými biomarkery. Dnes mají vědci k dispozici celou škálu různých barev povětšinou již geneticky modifikovaných fluorescenčních proteinů, které k tajemnému světélkování vybuzují fotony o různé energii, což umožňuje si pro konkrétní výzkum vybrat ten nejvhodnější marker. Když se jeho genetický kód vpašuje do řetězce DNA konkrétního genu, bílkoviny, jež produkuje, jsou obohaceny o fluoreskující oblast a ta je zviditelňuje. To umožňuje například přímo v živých organismech zkoumat aktivitu jednotlivých genů, šíření nádorových buněk, vývoj různých částí těla a orgánů v embryích pokusných zvířat, třeba tvorbu konkrétních neuronových sítí v mozku. Luminiscenční biomarkery nabízí bezpočet různých možností, dokonce i s komerčním cílem – v roce 1999 se na trhu objevily transgenní světélkující akvarijní rybičky, po nich přišly myši i kočky, prasátka, králíci...
Nejzářivější buňka
V nejnovějším čísle časopisu Nature Photonics americká dvojice Malte C. Gather a Seok Hyun Yun představuje netypický „laser tvořený jedinou živou buňkou produkující fluorescenční protein“ (citace z abstraktu článku). Nejde o příliš za vlasy přitažené přirovnání, vědci vskutku kombinací geneticky upravené buňky, do níž vpašovali program pro běžný zelený fluorescenční protein a optické soustavy vytvořili laser - tedy Light Amplification by Stimulated Emission of Radiation, což v překladu značí, že pomocí stimulovaného vyzařování zesílili budící světlo. Samozřejmě s výkonem ani jinými parametry běžných laserů se ten jednobuněčný nedá srovnávat a ani ho nelze pro tento účel použít. Jeho paprsek je sice úzký a směrovaný, tvořený hezkým, volným okem jasně viditelným zeleným světlem, jež ale není koherentní a má příliš malou intenzitu. I tak je asi desetinásobná, než jakou vyzařuje buňka medúzy, z níž fluorescenční protein pochází.
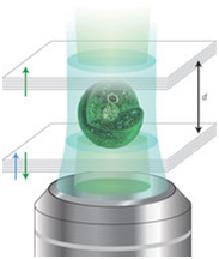
Kombinace buňky a optického rezonátoru
Malte C. Gather a Seok Hyun Yun si připravili živný roztok s obsahem geneticky modifikovaných jaterních buněk lidského embrya, které produkovaly zeleně fluoreskující protein. Pak jeho malou kapičku umístili na speciální Braggovo zrcadlo s průměrem 3 cm. Nad něj do vzdálenosti 200 mikrometrů umístili další, čímž vytvořili optický mikrodutinový rezonátor. V zorném poli mikroskopu oběma zrcadly manipulovali tak, až se jim podařilo šířku dutiny snížit na 20 mikrometrů a v ní zafixovat jedinou živou buňku. Systém pak ozařovali krátkými nanosekundy trvajícími pulzy modrého laserového světla. Obě optická zrcadla pomocí mnohonásobných odrazů zvýšily jeho působení na buňku, která v pohodě a bez poškození přežila stovku takových multiplikovaných pulzů. Vědci sérii pokusů testovali, jak fluorescenční protein reaguje, když budou intenzitu primárního laserového paprsku zvyšovat. Zjistili, že když jeho energie přesáhne 1 nJ (miliardtinu Joulu), intenzita zeleného záření prudce naroste a v jeho spektru se objeví jen několik úzkých, ale výrazných emisních vrcholů. To je podle autorů důkazem, že molekuly fluorescenčních proteinů jsou ve vybuzeném stavu a září ne díky spontánní, nýbrž stimulací vyvolané emisi fotonů. Tedy že systém se chová jako laser. Má zajímavou samoregenerační vlastnost. Když dojde k narušení proteinu s fluoreskující částí, buňka vyprodukuje jeho další molekuly.
Poznatek bez praktické aplikace. Zatím.
I když je to z hlediska poznání bezpochyby zajímavý výsledek, jeho praktické využití je otázkou bez konkrétní odpovědi. Nejpravděpodobnější význam by molekulární biolaser mohl mít v in-vitro výzkumu jednotlivých buněk. Podle předpokladů by se některé (všechny?) chorobné změny měly projevit na indexu optického lomu příslušného typu buněk. To by umožnilo pomocí analýzy jejich dostatečně intenzivní fluorescence rozlišit, jestli buňka uvězněná v optickém rezonátoru je zdravá, benigní, nebo maligní, anebo jestli není napadena virem.
Gather nahlas uvažuje i nad téměř sci-fi aplikací tohoto systému uvnitř těla. To ale vyžaduje, aby se optický mikrodutinový rezonátor zmenšil natolik, až by se mohl stát nitrobuněčnou strukturou. Samotná buňka by pak mohla působit jako autonomní mikrolaser. Jakékoli nitrotělní použití ale naráží na komplikaci – systém vyžaduje primární budící záření. U pokusných zvířat by se to dalo vyřešit například tenkými optickými vlákny zavedenými ke zkoumané tkáni. Ale to je předbíhání vývoje, který se s nemalou pravděpodobností neuskuteční.
Video 1: V teplém Rudém moři mnohé korály pod modrým světlem zeleně fluoreskují. Kredit: BBC Earth YouTube channel
Video 2: Objev zeleného fluorescenčního proteinu, rozdíl mezi bioluminiscencí a biofluorescencí a využití fluorescenčních proteinů v současném biologickém a genetickém výzkumu. Kredit: Virginia Commonwealth University
Zdroj: Nature News, Nature Photonics