
Vědci z Emory University School of Medicine dokázali odemknout mozkovou oblast o níž se předpokládalo, že není flexibilní. Vlastně přišli na to, že myši s neschopným genem RGS14 jsou schopnější. To, co si jejich geneticky upravená myš jednou prohlédne, snadněji si později vybaví a tak je pro ní cesta bludištěm snadnější. Máme tu tedy jakýsi paradox – normální (správná?) funkce genu omezuje paměť i učení. Gen snižující výkon mozku vědci nazvali RGS14. Polem jeho působení je zvláštní oblast v hipokampu.
RGS14
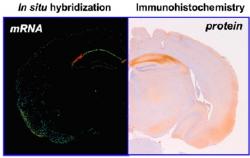
Gen s "poetickým" názvem RGS14 není jen výsadou myší, vlastníme ho i my, lidé. Kóduje protein (je stejného jména), který by se měl účastnit při zpracovávání signálů přicházejících do mozku. Zda v tom hraje klíčovou roli si vědci ověřili na myškách pomocí genové manipulace. Gen RGS14 jim poničili a následně pátrali, co tím provedli. Zásah se projevil v hipokampu - konkrétně v jeho části CA2. Jeho buňky začaly odpovídat i na slabé elektrické podráždění. Při tomto pátrání nešli vědci tak úplně naslepo. Z historie neurovědy je totiž známo, že oblasti hipokampu se účastní na dlouhodobé paměti a na posilování spojů mezi neurony, což je pro formování a vybavování si vzpomínek věc dosti podstatná. Ostatně i pokusy na samotných nervových buňkách pěstovaných v kultuře na Petriho misce vypovídají prakticky o tomtéž – gen RGS14 a jeho protein se na propojování neuronů a schopnostech jejich stimulace el. proudem účastní.
CA2
Oblast CA2 v hipokampu je ale poněkud zvláštním místem. Od svého okolí se liší tím, že se na dlouhodobé paměti nepodílí. Neurony v této oblasti jsou jaksi stranou veškerého dění, snadno přežívají zranění, záchvaty a mrtvičky. To neurony z jiných lokalit hippokampu nedokážou.
U myší s poničeným RGS14 genem došlo k výrazné změně. Jinak „líná“ CA2 oblast jakoby se probrala z letargie a byla najednou plná aktivity. Podráždění v ní mělo za následek vytváření mnohem silnějších spojů. To se projevovalo nejen na buňkách pěstovaných v kultuře ale i na chování živých myší. Provedeme-li rekapitulaci k čemu tady došlo tak můžeme konstatovat, že vyřazením genu z činnosti se spustila aktiita neuronů v oblasti hipokampálního mozku, oblasti CA2. Neurony si snadněji začaly vybavovat jak staré, tak i nové věci, rychleji začaly nacházet cestu z bludiště, snadno si vzpomínaly, kde se pod obarvenou neprůhlednou vodou v bazénku kdysi ukrývala plošinka na které se dalo odpočinout a vylepšila se jim i prostorová představivost.
Ničení a vylepšování
Něco v genomu nenávratně zničit genovým knokautem nemusí být vždy ke škodě. Na Floridské státní univerzitě takto myškám vyřadili gen pro protein nazývaný Kv1.3. Vytvořili myš, která ve srovnání se svými vrstevnicemi cítí pachy o deset tisíckrát slabší koncentraci.
Poničení genu se využívá i v praxi. Likvidací genu pro protein myostatin, který v organismu funguje jako růstový a diferenciační faktor brzdící růst svalů, lze připravit zvířata, jejichž svalová hmota je větší až o 20 %. Takový steak se nejen nevejde na běžný talíř, ale je dokonce zdravější, protože v takových svalech dochází k redukci obsahu tuku. Chovatelé skotu si také neztěžují, neboť takové zvíře lépe využívá krmivo a za stejné peníze toho "vyrobí" více.
Zásahů do dědičné informace, které mají u laboratorních myší za následek zvýšení „intelektu“ jsou dnes popsány desítky. Myši zmoudří například po potlačení funkce genu Cdk5 nebo naopak posílením činnosti genu Hras. Knokautováním genu se již dříve podařilo hlodavcům zlepšit krátkodobou paměť. Šlo tehdy o vyřazení genu pro tvorbu proteinu kalcineurin. Zásah způsobil, že elektrické signály v mozku mizely pomaleji a upravená myš si pamatovala vjemy z prostředí o několik dnů déle než její vrstevnice.

Proč?
Zapeklitou otázkou je, proč bychom spolu s myšmi (a zřejmě i dalšími živočichy) měli mít gen, který paměť omezuje. Pojistka bránící chytrosti je přece tak nelogická. Vědci si myslí, že by ve hře mohlo být zajištění rovnováhy zpracovávaných signálů. Pokud náš mozek pracuje podobně jako počítač, jeho výkon a kapacita jsou omezené a snadno by mohlo dojít k jeho zahlcení. Organismus si nemůže dovolit „nechat systém spadnout a provést reset“. Možná jsme tu narazili na něco, co by za jistých podmínek vylepšit přece jen šlo. Tak jako si na svém notebooku omezením výkonu počítače v jednom směru můžeme posílit jeho schopnosti řešit v dané chvíli úkoly jinde. To ale předbíháme, zatím jen víme, že vylepšit schopnost si věci zapamatovat lze a že spolu s tím jde vylepšit schopnost si nabyté zkušenosti vybavovat. Další potěšitelnou zprávou je, že se nepodařilo prokázat, že by vypnutí genu přivodilo hlodavcům nějakou újmu. Kromě zvýšené inteligence, ničím jiným pokusné myšky netrpí. Myslet si, že ani v budoucnu se na nic škodlivého nepřijde by ale bylo naivní. Možná by nám v tom mohli pomoci schizofrenici. Často jim totiž určitý typ neuronů v oblasti CA2 chybí. I když v jejich případě jde o zcela jiné geny, jistá souvislost se tu nabízí - fungování paměti a hipokampální oblasti CA2. Změna fungování oblasti CA2 u schizofreniků mění jejich sociální cítění a chování.
Dosud provedené pokusy na myších se agresivitě a sociálnímu chování nevěnovaly. V úvahu proto musíme vzít i to, že genový knokaut by z nás mohl udělat asociální chytrolíny. Stejně pravděpodobná ale je i varianta, že tomu tak nebude. Je o to lákavější, že vypínat a zapínat geny již molekulární mágové dovedou i jinými metodami. Utlumení „Simpsonova genu“ by se tedy v budoucnu mohlo provádět šetrněji a ne jako zde humpoláckou technikou genového knokautu bez možnosti vrátit věc zpět do původního stavu. Pro zapínání genu se zpravidla používá vložení silného promotoru, který zajistí úspěšný přepis genu. Omezení jeho funkce (transkripci) lze provádět například pomocí malých molekul RNA. Možností jak geny zapínat a vypínat je ale více. "Dolaďování" genů - jejich uspávání a probouzení není hudba budoucnosti, je zvládnutelná s již dnes odzkoušenými technikami. Náš mozek nebyl stvořen k dokonalosti a je velká škoda, že na vylepšování našich schopností se nesoustředí tolik pracovišť, mozkového trastu a prostředků, jako na oteplování.
Pramen: Emory University, PNAS 10.1073/pnas.1005362107
