Escherichia coli je miláčkem genetiků. Vědci jí nyní podstrčili do genomu uměle sestavenou sérii genů, s nimiž bakterie dokáže počítat. Základ takových počtů spočívá v registrování opakujících se dějů a reagování na ně. Jde o novou technologii, která umožňuje programovat buňky, aby dělaly věci, které ve svém plánu nikdy dělat neměly. V květnovém čísle časopisu Science se tomuto tématu věnuje tým pracovníků tří prestižních výzkumných pracovišť. Podle nich jde o technologii, kterou lze využít v praxi. Například k monitorování toxinů v prostředí. Nebo ke sledování buněčného dělení. Systém dovoluje naprogramovat buňky tak, aby se hlídaly a zahubily se, když začnou dělat neplechu.

Apoptóza
Systémy, které nám v buňce zajišťují „počty“, máme dány již od přírody. Příkladem je zkracování telomery, která je po každém dělení buňky kratší a kratší a když dosáhne kritické hodnoty, chromozomy se pomíchají a vznikne chaos, který buňku zahubí. Je to taková pojistka proti rakovině. Takovému chování buňky se říká řízená smrt čili apoptóza. Pravda je, že jsou rakoviny, které dokážou tento náš obranný systém oblafnout. Ale to by již bylo na jiný článek. My se nyní vrátíme k našemu synteticky vyrobenému „počítadlu“ a jeho možnostem.
Christina Smolkeová, bioiženýrka ze Stanford University se o nově vytvořené syntetické hříčce genetiků vyjádřila slovy: „Je to první případ syntetického počítadla v přírodě, jehož dopad si zatím neumíme představit“. Zatím ale syntetické genové počítadlo není žádný výkonný computer. Jde jen o systém genů, který umí počítat pouze do tří (zatím). Jde o uměle poskládané kousky DNA, které se vpašují do genomu organismu. V tomto případě šlo o bakterie, ale stejnou funkci mohou plnit v kterémkoli živém tvoru. Po vpravení do genomu se tato uměle vytvořená DNA struktura začne chovat tak, jak jí genetici předurčí – v našem případě začne reagovat, pokud se organismus setká s jedním cukrem a pokud se takové setkání opakuje, potom zajistí, aby se něco relevantního v organismu událo. Jde tedy o reakci na opakovaný (cyklický) děj.
Příprava umělé DNA spadá do zdárně se rozvíjejícího oboru syntetická biologie. DNA molekuly, o kterých zde mluvíme, byly sestaveny z několika genů tak, aby v buňce odpovídaly na specifické signály a aby po přijmutí takového signálu, se zahájila (nebo ukončila) syntéza proteinu. Pokusy v tomto směru probíhají již od 70. let, kdy poprvé vědci sestavili umělé buněčné „součástky“ a využili je k vylepšení živých tvorů. Vnášení genů je dnes na denním pořádku a známe ho z praxe například u bakterií produkujících biopaliva, konzumujících toxiny v zamořeném prostředí. Říkáme tomu tvorba geneticky modifikovaných organismů. V souvislosti s jejich rozšiřováním ale panují i obavy, že se jejich nové geny vymknou kontrole. Právě takové obavy z možného úniku geneticky modifikovaných organismů do přírody stály za snahou vytvořit umělé destrukční zařízení, které by v případě nutnosti buňky zničilo.
Strach z GMO stál za projekty syntetických úseků DNA, které by fungovaly jako „časovací zařízení“. Takovou DNA se nyní podařilo sestavit a lze jí vložit i do tak malého organismu, jakým je bakterie. Zařízení může být nastaveno například na počet dělení buňky, anebo na počet vystřídaných cyklů den/noc. Vkládání takových destrukčních zařízení by se mohlo v budoucnu stát zárukou, že se geny z GMO nebudou dál šířit.
Vedoucí výzkumného týmu James Collins se svými kolegy sestavil již dva systémy, které by k takovým cílům mohly být využity. Každý z nich registruje (počítá) odlišným způsobem, ale výsledkem jejich činnosti je spouštění kaskádovitých reakcí, na jejichž konci je tvorba nějakého významného proteinu – tedy funkce.
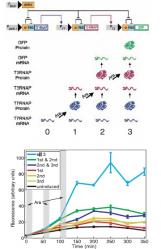
Pro demonstraci funkčnosti systému provedli vědci pokus, kdy do bakterie vnesli umělou DNA, jež sledovala opakované vystavení buňky vyšší koncentraci arabinózy. Celé to funguje tak, že pokud se buňka setká s tímto sacharidem ze skupiny pentóz, spustí se produkce specifického proteinu (první typ enzymu RNA polymerázy). Při druhém setkání buňky s „vlnou“ sladké arabinózy, se pak za přispění prvního proteinu vytvoří jiný, nový protein (druhý typ enzymu RNA polymerázy). Po třetím naservírování sladkostí druhý z vytvořených proteinů se zaslouží o vznik fluoreskujícího proteinu. To znamená, že buňka reaguje na každý cyklus (setkání s arabinózou) ale až po třetím kole zahájí tvorbu fluoreskujícího proteinu a zeleně se rozsvítí. Zelenkavou fluorescencí nám bakterie dávají na srozuměnou, že nějaký děj u nich proběhl tolikrát, na kolik cyklů jsme jim jejich syntetický DNA detektor nastavili. V tomto případě šlo o důkaz toho, že buňky evidují (počítají) kolikrát se dostaly do prostředí se zvýšenou koncentrací cukru. Zatím vědci naučili počítat buňky jen do tří. Úpravou délky vkládané syntetické DNA je brzo chtějí naučit vyšší matematice.

První „počítadlo“ je založeno na kaskádové syntéze různých typů RNA polymeráz. Druhé z vytvořených DNA „počítadel“ využívá sérii genů pro enzym DNA invertázu a jejich schopnosti specifického štěpení DNA. Když se buňka vybavená tímto typem počítadla poprvé setká se sledovaným signálem, spustí tvorbu prvního z enzymů. Ten rozštěpí svou vlastní DNA sekvenci a vloží ji zpět opačně. Tím ukončí svojí produkci a zároveň tím dovolí, aby se při druhém signálu spustila tvorba jiného enzymu (DNA invertázy), který rozštěpí jinou část DNA. Také na konci tohoto procesu je stejně jako v prvém případě, spuštění genu, který zahájí tvorbu proteinu s nějakou významnou funkcí (zde simulováno opět tvorbou zeleně fluoreskujícího proteinu).
Tento druhý systém, který k počítání cyklů využívá tvorby enzymů, může být naprogramován tak, že bude podávat informaci o tom, ve kterém stadiu se buňka nachází. Můžeme tedy průběžně "odečítat", kolikrát na sledovanou látku buňka natrefila. DNA invertáz je zhruba sto a také do tolika kroků může počítadlo pracovat. Pak se teoreticky může vynulovat a začít znovu.
Proč vědci tvořili dva nezávislé systémy? Inu proto, že ten první je vhodný pro sledování krátkých cyklů - rychle po sobě jdoucích události, jež se střídají v rozmezí zhruba 30 minut.
Druhý způsob evidence dějů – založený na enzymech zvaných DNA invertáza, je zase šitý na míru pozvolným dějům. Molekuly enzymů potřebují k rozvinutí svých stříhacích a slepovacích schopností více času a ideální je pro ně sledování cyklů probíhajících v rámci dnů.
Hraní genetiků s nastavováním detektoru a ovlivňováním základních buněčných procesů může vyústit v nespočet praktických aplikací. Některé bakterie mají ve svém DNA vybavení, jež má schopnost reagovat na světlo, arzen, teplotu, živiny anebo na přítomnost těžkých kovů. Dodání samotného „počítadla“ k těmto detekčním schopnostem je (pokud se to umí), relativně triviální záležitostí.
Organismy, dovybavené zmíněnými DNA detektory se mohou dál upravit aby vytvořili proteiny s roztodivnými funkcemi. Může se naprogramovat exploze jejich buněk poté, co dosáhnou stanovený počet cyklů. Buňky se mohou přinutit, aby se „protáhly“, nebo je naopak nechat ztloustnout, případně jim jejich růst zatrhnout zcela. Ve stávajících silách výzkumníků je již sestavení takového „DNA prográmku“, který zajistí, že tvorba fluoreskujících proteinů nám bude hlásit v jakém stádiu se nachází a kolikrát se s daným agens za svůj život setkala různou barvou. Po prvním podnětu mohou fluoreskovat žlutě, po druhém absolvovaném střetnutí červeně a ve finále třeba zeleně.
Kde všude se syntetická DNA se svojí schopností „počítat“ v budoucnu uplatní, se zatím můžeme jen dohadovat.
Prameny
V článku byly využity poznatky pracovišť: Howard Hughes Medical Institute, Department of Biomedical Engineering, Center for BioDynamics and Center for Advanced Biotechnology, Boston University, Boston.
Harvard-MIT Division of Health Sciences and Technology, Cambridge.
Department of Genetics, Harvard Medical School, Boston.