
Cystická fibróza je relativně častým dědičných onemocněním bělochů. V průměru je postiženo jedno na každých 2 500 živě narozených dětí. Onemocnění postihuje dýchací a trávicí trakt, přičemž plicní forma je u postižených také většinou příčinou jejich předčasné smrti. Jen ve Spojených státech je cystickou fibrózou postiženo asi 30 tisíc dětí a dospělých. Ve světě se počet postižených odhaduje na dalších 70 tisíc osob. Každoročně je diagnostikována zhruba tisícovka nových případů, přičemž více než 70 % pacientů je odhaleno ve věku do dvou let.
Ještě v padesátých letech dvacátého století se pouze několik málo dětí dožilo zahájení školní docházky, avšak díky postupujícímu výzkumu a modernějším lékům je v současnosti více než čtyřicet procent pacientů starších osmnácti let a průměrná délka života postižených osob se zvýšila na 36 let a dá se počítat s jejím dalším prodlužováním. Díky nedávno vyvinutým lékům a speciální péči mají osoby postižené cystickou fibrózou větší možnost kontroly nad svou nemocí. Díky tomu žijí tito nemocní nejenom déle, ale hlavně se jejich život se stává o něco kvalitnějším.
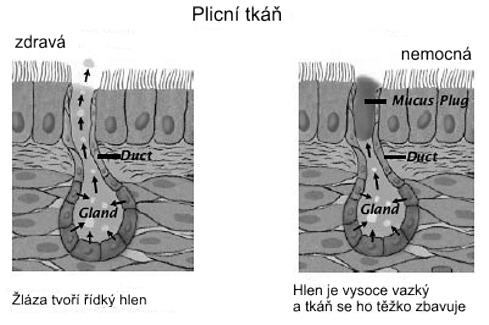
Ve zdravých plicích dochází k vylučování a následnému odstraňování hlenu, což čistí průdušnice a průdušinky a tak napomáhá v boji proti infekcím. Cystická fibróza způsobuje ucpání žlázek vylučujících hlen, tím dochází nejenom ke zhoršení dýchání, ale plíce hlavně ztrácí svou schopnost samočištění a tak jsou postupně ničeny bakteriálními infekcemi (obr.: Iroquois Home Care)

Již roky vědci studující cystickou fibrózu využívají pro výzkum nových preparátů na tuto nemoc myši, u kterých byl pozměněn gen odpovědný za cystickou fibrózu. Avšak má to jeden velký háček, dalo by se spíše říci pořádný hák – u myší se nevyvíjí cystická fibróza s jejími příznaky plicního onemocnění, tak jako u člověka.
Výzkumníci z University of Missouri a University of Iowa se rozhodli opatřit si vhodnější modelové zvířete, které by vyhovovalo jejich potřebám a které by mohlo přesně napodobit projevy cystické fibrózy u lidí. Z mnoha důvodů padla volba na prase.
Randal Prather, profesor reprodukční biotechnologie na MU College of Agriculture, Food and Natural Resources, spolupracoval s Michaelem Welshem z Howard Hughes Medical Institute na University of Iowa. Tým vedený Welshem provedl genetické modifikace, kterým zmíněný defekt v prasečích buňkách vyvolal. Pratherova skupina potom z těchto pozměněných buněk, za použití metody přenosu jader, vytvořila geneticky modifikované klony prasat. Vědci doufají, že touto genetickou modifikací budou schopni napodobit plicní onemocnění, které postihuje osoby trpící cystickou fibrózou.
Prasata, která byla genetickou manipulací vytvořena, nesou pouze jednu sadu mutovaných genů. Cystická fibróza ale propuká pouze v případě, když organismus má poškozený gen v obou chromozomálních sadách. Proto Prather chová tato zvířata a záměrnou příbuzenskou plemenitbou získává potomky s oběma defektními geny. Selata u nichž by mělo dojít k projevu nemoci se mají rarodit na jaře příštího roku. Potom už jen vědce čeká ověřit, zda i prasat bude mít poškození genů stejné důsledky, jako tomu je u lidí.

Gen zodpovědný za cystickou fibrózu se u lidí vyskytuje na chromozómu č. 7. U většiny (zhruba 70 procent) pacientů s cystickou fibrózou je defekt způsoben chyběním (delecí) tří nukleotidů. Nejčastěji jde o vypadnutí tří písmen genetické abecedy (viz červeně orámovaná část představující sekvenci C T T ). Zmizení těchto tří písmen způspobí, že tato vadná genetická předloha dá vznik poněkud kratšímu proteinu s jinými vlastnostmi. Takto pozměněnému proteinu totiž bude v pozici 508 chybět aminokyselina fenylalanin. Dodatečně se zjistilo, že kromě této zde popsané nejčastější příčiny (výpadek tripletu Cytosin Thymin Thymin) se stejná choroba (cystická fibróza) vyvine i u některých dalších genetických poruch. Celkem již bylo objeveno přes 900 dalších mutací, které rovněž vedou k problémům zvaným cystická fibróza. (McGill Medicine Host Resistance)
Sledováním tvorby produktu tohoto genu, jímž je příslušný úsek mRNA se ukázalo, že gen se zapíná a plní nějaké funkce v buňkách pankreatu, plících, tlustém střevu, potních žlázách a játrech. Na úrovni proteinu lze jeho činnost vystopovat molekulou složenou ze 1480 aminokyselin. Tento protein byl nazván CFTR protein. O tomto proteinu se někdy také hovoří jako o transmembránovém regulátoru vodivosti. To proto, že zmíněný protein je součástí vnější části buněčné membrány. Důsledkem jeho porušené struktury je tvorba nezvykle vazkého sekretu a potu s vyšším obsahem soli.

„Gen, jehož poškození má na svědomí cystickou fibrózu byl objeven už v roce 1989. Dosud ale na ní stále nerozumíme mnoha věcem a tak naše léčba zůstává málo účinnou,“ řekl Welsh. „Ačkoliv se vědci a lékaři již na myších naučili mnoho, k dalšímu pokroku potřebujeme zvíře, u kterého budou alespoň zčásti napodobeny lidské projevy plicního onemocnění. Krom toho pracujeme i s dalšími výzkumníky z University of Iowa, kteří dělají podobnou práci s fretkami. Doufáme, že naše cesty konečně poskytnou zdravotníkům modelové zvíře které pomůže lidem trpícím cystickou fibrózou usnadnit jejich úděl.“
Produkce těchto prasat by mohla přispět k vývoji nových léků a zajistit tak účinnou léčbu, která dosud není možná. Jen pro zajímavost, vědci již vytvořili více než jedenáct typů modelových myší ke studiu cystické fibrózy, avšak u žádné z nich se nevyvinuly spontánně její plicní projevy.
„Věříme, že toto je cesta, která by mohla vést k postupnému širšímu využití prasat při studiu dalších nemocí u kterých se nedaří najít vhodný experimentální model“ říká Prather. „Prasata jsou v mnoha ohledech velmi podobná lidem a mohou se stát oním pomyslným „klíčem“ pro nalezení léků a léčebných metod na mnoho našich nemocí.“
Zdroj: University of Missouri-Columbia, Cystic Fibrosis Foundation, (McGill Medicine Host Resistance)