Tělo denně nahrazuje asi 330 miliard buněk (zdroj). V takovém počtu se nejednou objeví mutacemi zparchantělá buňka, jež má schopnost se nekontrolovatelně dělit a stát se tak zárodkem rakovinového bujení. V drtivé většině případů se nic nestane, protože neunikne včasnému zákroku ostražitého imunitního systému, který ji zničí.
Otázky proč a jak se některá nádorová „semínka“ imunitní ochraně ubrání, jsou důležitým cílem onkologického výzkumu. Rozsáhlého a složitého, jako jsou i mechanizmy, kterým zhoubný proces vzniká. Jeho výsledkem je buď solidní (pevný, kompaktní, angl. solid) zhoubný nádor – víceméně ohraničená nádorová tkáň, jako například při rakovině prsu, anebo tekutý (hematologický, angl. liquid) karcinom, označovaný často jako rakovina krve. Vyvíjí se v krvi, kostní dřeni nebo lymfatických uzlinách a projevem je leukémie, lymfom, nebo myelom.
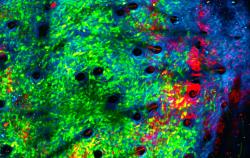
Všichni víme, že onkologická léčba je spjatá s chemoterapií a ozařováním, jež cílí přímo na rakovinné buňky. Intenzivně se bádá také na poli imunoterapeutických léků, kterými se lékaři snaží nastartovat agresivnější imunitní útok na smrtelně nebezpečného, zpod kontroly uniklého záškodníka. Stimulovat imunitní systém nemusí jen léky. Dokazuje to zajímavá studie vědců převážně z australského Garvanova ústavu lékařského výzkumu (Garvan Institute of Medical Research). Tato biomedicínská výzkumná společnost se sídlem na předměstí Sydney, v Darlinghurstu, slaví letos 60. výročí svého založení. Tehdy jen výzkumné oddělení Nemocnice sv. Vincenta se mezičasem rozrostlo v institut o velikosti naší menší nemocnice. Zaměřuje se na širší spektrum chorob, nejen na rakovinu.
Na stránce Garvanova ústavu se před několika dny objevila mediální zpráva „Vystavení rakoviny bakteriím připomíná imunitním buňkám první reakce, na čí straně jsou“. Stručně přibližuje výsledky studie zveřejněné v odborném časopisu Cancer Research, v níž 14členný tým vedený šéfkou Laboratoře vrozené a nádorové imunologie Garvanova ústavu Tatyanou Chtanovou prokázal, že cílené infikování solidního nádoru vhodným patogenním organismem může zmobilizovat některé imunitní mechanismy k útoku proti rakovinným buňkám. A to přesto, že předtím působily spíše k jejich prospěchu.

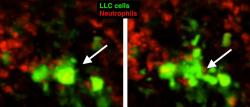
Pokusům byly vystaveny laboratorní myšky chované v sterilním prostředí bez patogenů. Vědci několika z nich do ušních boltců zanesli buňky Lewisova karcinomu plic, myšího typu rakoviny, kterou lze mezi pokusnými hlodavci uměle šířit pomocí transplantace. Samozřejmě výhradně pro vědecké účely. Výzkumníci sledovali růst nádoru a interakce jeho buněk s buňkami imunitního systému. Když karcinom dosáhl určité velikosti, vstříkli do něj injekce s buňkami inaktivovaného zlatého stafylokoka (Staphylococcus aureus), běžně se vyskytující bakterie, kterou byste s velkou pravděpodobnosti objevili i na vlastní pokožce. Tento, myším organizmům cizorodý a jejich imunitnímu systému, který dozrával v sterilním prostředí, neznámy patogen, vybudil imunitní reakci. V jejím důsledku se slabší (subakutní) zánět, typický pro většinu zhoubných solidních nádorů, změnil na intenzivní, akutní formu. Snad se to jeví jako zhoršení zdravotního stavu, ale opak je pravdou. Většina solidních nádorů totiž ve své i okolní tkáni vyvolává chronickou, sobě paradoxně prospěšnou zánětlivou odezvu, která podporuje tvorbu krevních kapilár, tím i výživu tumoru a zároveň potlačuje imunitní obranu působící proti němu. Silnější akutní zánět, jenž je reakcí na injekce se stafylokoky, vede k rychlým a dramatickým změnám. Aktivuje zejména neutrofilní granulocyty, zkráceně neutrofily – druh bílých krvinek, jejichž důležitým úkolem je fagocytóza čili pohlcování cizorodých částic, mikrobů nebo poškozených buněk, i těch rakovinných. (Pod textem najdete krátké, srozumitelné video o činnosti neutrofilů i s českým překladem titulků).
Infekce nádoru oslabenými stafylokoky tedy lokálně zmobilizovala imunitní systém, z neutrofilních granulocytů k nádoru přátelských se stali válečníci požírající jeho buňky. Proměna chování neutrofilů souvisí se změnami aktivity některých jejich genů, v důsledku čehož začnou také produkovat molekuly, které chemicky přilákají další důležité pomocníky – T-lymfocyty. Jsou, podobně jako neutrofily, druhem bílých krvinek s obrannou funkcí. Zatímco podtyp TH1 působí zánětlivě, buňky Tc pomáhají neutrofilům ničit buňky nádoru tím, že iniciují jejich buněčnou smrt – apoptózu.
I když princip ovlivňování imunitního prostředí kompaktního nádoru pomocí mikrobů může časem dospět v terapii vhodnou pro humánní medicínu, stěží bude „samospasitelnou“. Jejím potenciálem však je stát se účinnou podpůrnou metodou k jiným způsobům imunoterapie, případně v součinnosti s chemo- a radioterapií. Nadějné výsledky se zatím dosáhly u zvířecích modelů pro karcinom plic, určité formy rakovinu prsu (triple negativní karcinomy prsu), pro melanom nebo rakovinu pankreatu.
##seznam_reklama##
Volně přístupný článek zveřejněný na stránkách časopisu Cancer Research, v závěrečné části Doplňkové údaje (Supplementary data) nabízí 4 krátká videa dokumentující jako neutrofily v tumoru „infikovaném“ stafylokoky interagují s nádorovými buňkami Lewisova karcinomu plic. Pojem „blebbing“ v názvu 4. videa souvisí se vznikem nepravidelných záhybů plazmatické membrány buněk, tzv. blebů, způsobených rozvolněním cytoskeletu. Zpravidla jde o ranou fázi buněčné smrti (apoptózy).
Poznámka pod čarou:
Uvádět, že rakovina je druhou nejčastější příčinou úmrtí a že tuto diagnózu si každoročně vyslechne kolem 90 tisíc obyvatel České republiky, je opakováním známých faktů (statistiky zde). Do výzkumu, jehož cílem je hledat nové nebo efektivnější terapeutické metody, tečou nemalé peníze. Pro ilustraci: americký National Cancer Institute (NCI – Národní onkologický ústav) požadoval pro tento fiskální rok z federálního rozpočtu 7,8 miliardy dolarů, o asi 800 milionů víc, než byl jeho loňský rozpočet (zdroj).
Onkologický výzkum v ČR zastřešuje loni otevřený Národní ústav pro výzkum rakoviny [NÚVR], který propojuje 11 významných pracovišť v Praze, Brně a Olomouci (zdroj). Hospodaří s obnosem 1,4 miliardy korun z evropského programu EXCELES.
Video 1: Neutrofilní extracelulární past
Překlad mluveného textu:
Neutrofil (neutrofilní granulocyt) je mocný a ostražitý obránce, který neustále slídí po krevním řečišti a hledá patogenní vetřelce. Když narazí na cíl, tento nenasytný požírač ho rychle pohltí a stráví. Po usmrcení kořisti tento lovec udělá něco nečekaného – nahodí síť, aby chytil další. Neutrofily jsou efektivní zabijáci, kteří očekávají, že zemřou, nikoli, že se budou rozmnožovat. Svou DNA využívá jako jednu ze zbraní, jichž má několik. Při setkání s patogenem neutrofil aktivuje enzym PAD4, který pevně svinutou chromozomální DNA rozbalí do volných vláken lepkavého materiálu podobného pavučině. Jaderný obsah je z neutrofilu vyvržen a vytvoří smrtící síť složenou z vláken DNA propojených histony a napuštěnou smrtícími antimikrobiálními látkami včetně myeloperoxidázy, neutrofilní elastázy a defensinů. Nově vytvořená síť je nastavena tak, aby zachytila a zabila všechny invazní bakterie, které mají tu smůlu, že vplují do jejího objetí. Po splnění svého úkolu musí být toxická síť deaktivována a zničena. Jádro rozporcuje DNA síť na menší fragmenty, které mohou být snadno pozřeny. Do oblasti se přesunou makrofágy a zlikvidují zbývající fragmenty sítě, čímž odstraní všechny stopy po patogenní infekci. Naneštěstí tento způsob obrany má dvě strany. Neúplné odstranění fragmentů sítě může vést k tvorbě autoprotilátek namířených proti složkám sítě včetně histonů, DNA a PAD4 (složek vlastních neutrofilních granulocytů). Tyto autoprotilátky mohou nakonec vést k rozvoji autoimunitních onemocnění jako je systémový lupus erythematodes nebo revmatoidní artritida.
Histony jsou shluky osmi proteinů, které tvoří podpůrnou „páteř“ chromosomů – kolem histonů se ovíjejí vlákna DNA, čímž chromozom získá kompaktní uspořádaný tvar. Histony také hrají roli v regulaci genové exprese.
Autoprotilátka – protilátka (imunoglobulin) namířená proti antigenům vlastního organismu
Video 2: Nádorová imunologie a imunoterapie
Delší, ale srozumitelné a poučné video: Jan Černý: Rakovina - chyba v matrixu (PřF UK 7.1.2023)
Literatura: Cancer Research, Garvan Institute of Medical Research