Léky na bázi ranitidinu (Zantac, Coralen, Gastrial, Taural atd.) patří do skupiny tzv. blokátorů histaminového receptoru H2 (H2 blokátory), které potlačují sekreci žaludečních kyselin, a tak ulevují při pálení žáhy či překyselení žaludku. Nejpravděpodobnějším zdrojem genotoxických N-nitrosaminů je v tomto případě rozklad účinné látky při dlouhodobém skladování za vysokých teplot. Stejný kontaminant byl v nadlimitních hodnotách nalezen také v metforminu, což je API určená ke snižování hladiny glukózy v krvi. N-nitrosaminy byly detekovány pouze v některých lécích, které danou API obsahovaly, v jiných nikoli. Zdá se tedy, že NDMA vzniká reakcí metforminu s některou z přídatných látek obsažených ve finálních lékových přípravcích. Další zástupci N-nitrosaminů 1-metyl-4-nitrosopiperazin (MNP) a 1-cyklopentyl-4-nitrosopiperazin (CPNP) kontaminovaly antibiotika rifampin a rifapentin používaná k léčbě tuberkulózy. Tento výčet není zdaleka konečný, má jen ukázat, že jde o problém, který není omezen na jednu účinnou látku, či lékovou skupinu.
První doklad o syntéze nitrosaminů pochází z roku 1874. Německý chemik Otto Nicolaus Witt (1853-1915) je vytvořil reakcí kyseliny dusité (HNO2) se sekundárními a terciálními aminy. Spojením nitrosylové (-N=O) skupiny s aminy (-NH2) vznikají látky obsahující N-nitrosaminovou skupinu (=N-NO), které v lidském organismu podstupují metabolickou přeměnu katalyzovanou jaterními enzymy (zejména Cytochrom P450 2E1) a uvolňují reaktivní částice (karbeniový CH3+ či alkylkarbeniový R-CH2+ ion, formaldehyd HCHO apod.) schopné se vázat na dusíkaté báze v DNA. V dané souvislosti se zdá být poměrně zajímavé, že hladinu příslušného biotransformačního enzymu v játrech ovlivňuje přítomnost etanolu a konzumenti alkoholu jsou tak ve větším zdravotním riziku než abstinenti.
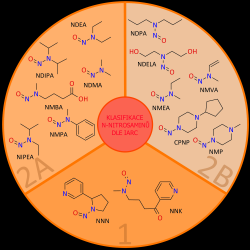
Ne všechny nitrosaminy podstupují danou přeměnu stejně ochotně a tudíž se liší i jejich nebezpečnost. Podle klasifikace Mezinárodní agentury pro výzkum rakoviny (IARC) patří do skupiny prokázaných lidských karcinogenů (kategorie 1) dva zástupci N-nitrosaminů, a to N' -nitrosonornikotin a 4-(metylnitrosamino)-1-(3-pyridil)-1-butanon. Mezi karcinogeny třídy 2A, tedy pravděpodobné lidské karcinogeny, patří 6 nitrosaminů včetně N-nitrosodimetylaminu (NDMA) a N-nitrosodietylaminu (NDEA), které jsou doposud nejčastěji prokázanými kontaminanty léčiv. Stejný počet látek s danou funkční skupinou pak bylo klasifikováno jako možné lidské karcinogeny (třída 2B).
Kontaminovaná léčiva samozřejmě nejsou jediným a ani hlavním zdrojem N-nitrosaminů pro lidský organismus. Nejvyšší úrovně expozice této skupině látek jsou spojeny zejména s kouřením, konzumací uzenin a pitím vody znečištěné dusíkatými látkami. V posledním jmenovaném případě se na tvorbě N-nitrosaminů významně podílejí střevní bakterie. Dalším významným endogenním zdrojem této skupiny látek jsou též zánětlivé procesy. Přestože je tedy náš organismus vystaven účinku N-nitrosaminů na denní bázi, vyvolalo zjištění jejich přítomnosti ve farmakologicky aktivních látkách poměrně velkou pozornost celé řady regulačních orgánů. Evropská léková agentura (EMA) stanovila v roce 2019 dočasný limit pro akceptovatelný denní příjem N-nitrosaminů z léčiv na úrovni 26.5 a 96 nanogramů/den, první limit byl odvozen z údajů o karcinogenitě NDEA, druhý pak z údajů o NDMA.
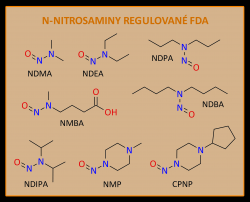
Podle aktuálního stanoviska FDA se limit 96 ng/den vztahuje také na N-nitroso-N-metyl-4-aminomáselnou kyselinu (NMBA) a limit 26.5 ng/den na N-nitrosometylfenylamin (NMPA), N-nitrosoisopropyletylamin (NIPEA) a N-Nitrosodiisopropylamine (NDIPA). Mezi lety 2019 až 2021 bylo v USA kvůli překročení výše zmíněného limitu staženo více než 1400 lékových přípravků, z nichž většina obsahovala účinnou látku valsartan, irbesartan nebo losartan, tedy léčiva učená k léčbě vysokého krevního tlaku ze skupiny blokátorů receptoru AT1 pro angiotensin II. Následují výše zmíněná léčiva metformin a ranitidin a dále antacidum nizatidin.
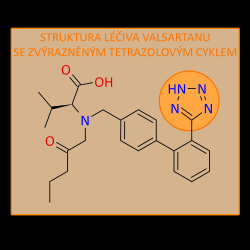
N-nitrosaminy vznikají zejména reakcí sekundárních či terciálních aminů s dusitany v kyselém prostředí. Aminy mohou při syntéze farmakologicky účinné látky sloužit jako základní reaktanty, dále mohou vznikat jako žádoucí či nežádoucí meziprodukty, případně může jít o kontaminanty jiných surovin. K syntéze celé řady léčiv se používají azidy. Dusitany se pak používají k odstranění nezreagovaného přebytku těchto azidů z reakční směsi. Dále se vyskytují jako běžný kontaminant některých chemikálií a také vody. Zdrojem N-nitrosaminů mohou být též látky používané k čištění výrobních linek, mohou vznikat reakcí farmakologicky účinné látky s dalšími složkami léčivého přípravku, dále při interakci léčiva s obalovým materiálem či rozpadem léčiva při dlouhodobém skladování v nevhodných podmínkách. Cestou ke snížení rizika kontaminace je tedy zejména kontrola kvality surovin, čištění vody a úprava technologického postupu tak, aby nedocházelo ke kontaktu aminů s nitrosační směsí. Poslední ze jmenovaných přístupů se ukázal být velmi účinný např. při syntéze sartanů, které ve své struktuře obsahují tetrazolový kruh. Formování této strukturní jednotky je totiž kritickým krokem, při němž dochází k tvorbě N-nitrosaminů a nebezpečí jejich vzniku může být významně redukováno, pokud zavedení tetrazolového kruhu do molekuly léčiva není posledním krokem syntézy.
##seznam_reklama##
Některé N-nitrosaminy vykazují pří testech na buněčných kulturách (in-vitro) genotoxický potenciál a vyvolávají vznik zhoubných nádorů u laboratorních zvířat. Jak je to ale se skutečným zdravotním rizikem spojeným s přítomností tohoto typu kontaminantu v léčivech? Z analýzy dat provedené EMA vyplývá, že na každých 100 000 pacientů léčených maximálními terapeutickými dávkami valsartanu s nejvyšší zaznamenanou mírou kontaminace NDMA po dobu šesti let připadne oproti přirozenému pozadí navíc 22 případů rakoviny. V případě, že by byl valsartan kontaminován maximálními zjištěnými koncentracemi NDEA a léčba by trvala pouze čtyři roky, přibylo by oproti pozadí 8 případů rakoviny. Daný problém má však i druhou stránku – u pacientů s diabetem II typu, kteří užívají metformin bylo zjištěno nižší riziko vzniku zhoubných nádorů než u pacientů, kteří dané léčivo neužívají. Pokud by snaha redukovat množství N-nitrosaminů v dané farmakologicky účinné látce vedlo k její nedostupnosti, mohlo by se paradoxně riziko vzniku nádorů u těchto pacientů zvýšit.
(Děkuji Petru Leinweberovi za zpracování obrázků)
Literatura:
-
U.S. Food & Drug Administration. 2020. FDA requests removal of all ranitidine products (Zantac) from the market. Press Release. Available at: https://www.fda.gov/news-events/press-announcements/fda-requests-removal-all-ranitidine-products-zantac-market.
-
European Medicines Agency. 2020. Suspension of ranitidine medicines in the EU. Press Release. Available at: https://www.ema.europa.eu/en/news/suspension-ranitidine-medicines-eu
-
European Medicines Agency (EMA), 2019b. Temporary interim limits for NMBA, DIPNA, and EIPNA impurities in sartan blood pressure medicines. EMA/351053/2019. https://www.ema.europa.eu/en/documents/other/temporary-interim-limits-nmba-dipna-eipna-impurities-sartan-blood-pressure-medicines_en.pdf
-
Tuesuwan, B. and V. Vongsutilers, Nitrosamine contamination in pharmaceuticals: Threat, impact, and control. Journal of Pharmaceutical Sciences, 2021. 110(9): p. 3118-3128
-
Bharate, S.S., 2021. Critical analysis of drug product recalls due to nitrosamine impurities. Journal of Medicinal Chemistry, 64(6), pp.2923-2936
-
Thresher, A., Foster, R., Ponting, D.J., Stalford, S.A., Tennant, R.E. and Thomas, R., 2020. Are all nitrosamines concerning? A review of mutagenicity and carcinogenicity data. Regulatory Toxicology and Pharmacology, 116, p.104749.
Redakce si dovolila připojit jedno autorovo video: