Co je CD47?
Název pochází z anglického Cluster of Differentiation, ale někde mu říkají s integrinem spojený protein. Je součástí buněčné membrány a účastní se celé řady procesů - apoptózy, proliferace, adheze, migrace,… . Nás dnes bude zajímat jeho klíčová role v imunitní odpovědi. Vykukuje na povrch všech zdravých buněk lidského těla a funguje jako vstupenka do kolektivu. A nebo chcete-li, tak jako razítko v občance z něhož je patrné, zda jde o spořádaně pracujícího občana, nebo migranta. V komunitě buněk je ochrana vlastního zvlášť úzkostlivě střežena a kontroloři jsou pořádní kruťáci. Kdo se takovému makrofágovi správně neprokáže, toho pozře a svým enzymovým šrotovníkem pomalu rozebere. Proto zdravé buňky ze své membrány vystrkují „nápis“ CD47 a jakoby jím bílým krvinkám neustále mávaly před nosem. Důvod je prostý, v tamní mluvě se to překládá jako „nejez mne“.
Někdy se to ale celé zvrtne a ochranný signál si osvojí i sobecké zvrhlé buňky, které to s naším tělem nemyslí dobře. To pak máme zaděláno průšvih. S maskovanými zvrhlíky si naše domobrana přirozené imunity neporadí. Za čas je neproduktivních jedlíků moc a integrita toho co fungovalo, bere za své, říkáme tomu rakovina.
Dnes si povíme o poznatku kolektivu onkologů čínsky znějících jmen z Chicaga. Pod vedením profesora Yang-Xin Fu experimentovali na myších sužovaných rakovinou. Nebyly to myši obyčejné, ale geneticky modifikované tak, aby co se CD47 týče, byly co nejpodobnější lidem. Zjišťovali na nich, zda a jak střevní mikroflóra jim je v nemoci ku prospěchu.
Nejprve ale něco málo teorie
Aby se imunitní systém s příživnickými individui prokazujícími se falešným „CD razítkem“ byl schopen vypořádat, je potřeba s jejich kamufláží něco udělat. Smýt anebo ji nějak vytrhat se nedaří, sahá hluboko a drží pevně. Proto V poslední době imunologové přišli s geniálním řešením. Vymysleli techniku léčby zvanou „anti-CD47 imunoterapie“. Přeloženo do lidštiny, na rakovinových buňkách se provede kamufláž kamufláže. Do nádoru se vpraví protilátky, které falešné razítko na membráně zvrhlých buněk zalepí. Makrofágy tak zprávu „nejez mne“ nepřečtou a přestanou okolo zvrhlíků chodit jak okolo horké kaše, a začnou konat, co mají v popisu práce. Jde o velice sofistikovanou, moderní a účinnou léčbu. Má však své mouchy. Některá pracoviště s ní tak dobré zkušenosti nemají. Léčba někdy nezabírá, ač by měla.

Vědátoři z Chicaga se svými kolegy z Dallasu, se proto vrátili k myšímu modelu a provedli řadu testů. Teď se teprve dostáváme k tomu podstatnému. Když své chlupaté pacientky krmili tak, aby v zažívacím traktu měly hodně bifidobakterií, nejen, že měly bakterie ve střívkách, ale ony si klíďo píďo, cestovaly i mimo střevní trakt. Už to je překvapivé, neboť slizniční bariera není žádný cedník. Imunitní aparát jakoby nad tím mhouřil oči, jak si bakterie ze zmíněné bariéry dělají bžundu. Ještě překvapivější na tom je, že tělem se potulující bakterie se kumulovaly v tumorech. A teď pozor, přichází finále. V nádorem změněné tkáni, tyto bifidobakterie silně stimulovaly léčbu zvanou anti-CD47 imunoterapie.
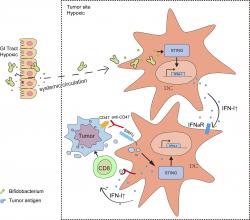
Vědci vše popsali slovy své vlastní hantýrky: Zablokováním CD47 se zlepšila křížová prezentace v dendritických buňkách s následnou stimulací genů majících pod palcem produkci interferonu. Ať už tomu ale budeme říkat aktivace proteinu STING, nebo lidově „naprasení se anaerobních bakterií do nádoru s provokačkou interferonu“, hlavní je, že myši, které předtím na léčbu nereagovaly, se mění na takzvané „odpovídače“, a jak autoři píší, začaly spolupracovat a jejich léčba byla úspěšná. Jinak řečeno, můžeme považovat za prokázané, že dieta upravující prostředí zažívacího traktu, aby v něm byly hojně zastoupené bifidobakterie, zvyšuje účinek léčby a šance na uzdravení.
Že jste o blahodárném účinku střevní mikroflóry při léčbě rakoviny už slyšeli?
To je možné, ba pravděpodobné. Ale zcela určitě ne v tomto kontextu. Doposud se totiž ve všech odborných publikacích uvádělo, že: Příznivé zdravotní účinky, jsou dílem regulace střevní mikrobiální homeostázy. Inhibicí patogenů a škodlivých bakterií, které kolonizují a infikují střevní sliznici. Že jde o dílo modulace lokálních a systémových imunitních odpovědí, potlačení prokarcinogenních enzymatických aktivit v mikrobiotě, nebo že jde o produkci vitamínů a biokonverze řady potravin sloučeniny na bioaktivní molekuly. Případně se psalo, že bifidobakterie zlepšují střevní slizniční bariéru tím, že snižují hladinu lipopolysacharidů ve střevě. Když to zkrátíme, tak vždy se předpokládalo, že jde o záležitost střev. Teprve až nynější pokusy odhalují, že hlavní efekt je někde jinde. Že jde o efekt až v nádorové tkáni a že v tom má prsty mechanismus, který se střevem prakticky nic společného nemá.
Může pospaný stimulační efekt imunoterapie u myší rakoviny být přínosem i pro nás, lidi?
Podle vědců může. Není totiž důvod předpokládat, že by popsaný efekt neměl fungovat i u méně ochlupených savců. I když léčba rakoviny probiotikem může dělat dojem šarlatánství, výsledky pokusů ukazují, že v případě léčby rakoviny nezáleží jen na tom, co nosíme v hlavě a jak jsme odhodláni se s osudem poprat, ale i na tom, co nám hlavou jen prochází a nosíme, takříkajíc proklatě nízko. To, že se vědci nemýlí a že za pozorovaným léčebným efektem skutečně stojí bakterie, potvrdily pokusy s antibiotiky. Když s jejich pomocí myškám bakterie vymýtili, léčba anti-CD47 imunoterapie přestala být účinná. Američtí vědci se už nechali slyšet, že teď se pustí do prověřování, zda kromě bifidobakterií, by nám při léčbě rakoviny nemohla být nápomocna i některá z dalších mikrobiot.
Závěr
Výsledky pokusů jsou jakýmsi apelem, abychom věnovali větší pozornost našemu „druhému já“, jak se střevnímu mikrobiomu také říká. U pacientů léčených imunoterapií tyto nové poznatky ale nastolily problém. V praxi se u nich často aplikuje preventivní antibiotická clona. Až na případy, kdy to bude vyloženě nutné, by se s ní teď mělo začít šetřit, neboť antibiotika svým vedlejším efektem nás připravují o přátelské bakterie, které nám jsou v demaskování rakovinou zvrhlých buněk nápomocny.
Literatura
Yaoyao Shi, et al.: Intratumoral accumulation of gut microbiota facilitates CD47-based immunotherapy via STING signaling. J Exp Med (2020) 217 (5): e20192282. https://doi.org/10.1084/jem.2019228