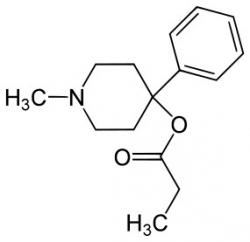
Začalo to morfinem
Druhé světové válce se někdy říká také drogová válka. Wehrmacht i luftwafe během druhé světové války dopovaly své frontové vojáky pervitinem. Spojenci zase zvyšovali mužstvu výkonnost amfetaminem Benzedrin, o němž je známo, že zvyšuje pocit blaženosti a nadřazenosti. Jeden z materiálů z let 1925–1930 dokládá, že jen v Německu se tehdy vyrobilo 98 tun morfinu. Inu, v dobách předválečných a válečných je o všechny životabudiče velký zájem. A po válce zase zůstává v pamětech přeživších tolik hrůzy, že poptávka po opioidních analgetikách neustává. Není se proto co divit, že zdravotnicko-chemické firmy měly snahu i v míru trh uspokojit. V laboratořích firmy Hoffmann-La Roche tak například vznikla syntetická látka se 70% účinností morfinu. Šlo o desmethylpropin (1-methyl-4-fenyl-4-propionoxypiperidin). Ve známost vešel jako MPPP. To bylo ještě v době, kdy vědci zajímavé výsledky své práce publikovali se všemi podrobnostmi.
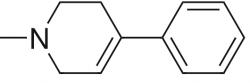
Proč se o tom zmiňujeme? Protože po zhruba třiceti letech, v plném rozmachu hnutí květinových dětí, napadlo Barry Kidstona, že by si rekreační zážitky mohl sám vyrábět a nemusel za ně utrácet. Jako student chemie se inspiroval ve třicet let staré publikaci o MPPP. Byl dost chytrý na to, aby se vyhnul případným námitkám patentového úřadu a uvařil si chemicky mírně odlišnou variantu - desmethylprodin. Několik měsíců ho na sobě s nadmírou spokojenosti testoval.
Jednoho dne ale byl hospitalizován s příznaky, které připomínaly již tehdy známou Parkinsonovu chorobu starců a stařen. Proč se objevily u studenta bylo záhadou. Podaný lék L-dopa (prekurzor dopaminu) mu od třesu ulevil, a tak bylo v diagnóze naprosto jasno. Mladík Parkinsona skutečně měl. Do té doby juvenilní parkinsonismus lékaři neznali.

Později vyšlo najevo, že se mladému výzkumníkovi nepodařilo vyrobit MPPP čistě a že ho měl kontaminované látkou zvanou MPTP (1-methyl-4-fenyl-1,2,3,6-tetrahydropyridin). Ta se ukázala být silným jedem. Tento jed je zvláštním typem neurotoxinu. Buňky si pečlivě vybírá. Ničí jen ty nervové buňky, které tvoří neuropřenašeč dopamin. Paradoxně tak Barry Kidstonovi lidstvo vděčí za mnoho. Jeho přičiněním dostali vědci do ruky nástroj, kterým si mohou ze zvířátek dělat parkinsoniky, kdy se jim zamane. A pak na nich zkoušet různé způsoby léčby. A to už začíná být hodně záslužná činnost. Parkinson je hned po Alzheimeru, druhá nejrozšířenější choroba neurodegenerativního onemocnění postihující mozek.
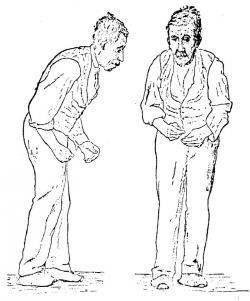
Parkinsonova choroba
O nemoci s příznaky této nemoci se zmiňují již papyry Starých Egypťanů. Taktéž různá pojednání z ájurvédy i poznámky starořeckého lékaře Galéna. Zmínku najdeme i v Bibli.
Jako "třaslavou obrnu" ji před dvěma sty lety popsal britský chirurg James Parkinson. Dnes už víme, že její příčinou je úbytek nervových mozkových buněk především v oblasti černá substance (substantia nigra). Je to místo, kde se tvoří přenašeč signálů mezi nervovými buňkami zvaný dopamin. Toho je nám třeba u několika nervových drah. Jedna z nich zajišťuje přenos signálů při plánování pohybu a jeho průběžné kontroly.

Třes ruky, prstu, brady nebo rtu.
Nejde jen o pohyb. Parkinson svým útlumem tvorby dopaminu se nám "postará" také o inkontinenci (u 50 % pacientů), zácpu (45 %), ztrátu čichu (90 %), dvojité vidění (10 %), pocení, impotenci (30 %), neurčité bolesti a deprese (30 %) i neschopnost radovat se z maličkostí a mít příjemné prožitky. Tomu psychologové říkají anhedonie. S tou se setká 30 % pacientů. V konečné fázi pak všechno a u všech završí demence.
Barry Kidston, experimentátor s raušem, dal svým počinem vědcům model, s jehož pomocí se jim nyní daří postupně nás zbavovat jednoho parikinsonického neduhu po druhém. Obstojně už lékaři zvládají deprese, zácpu, nadměrné pocení i vylepšení čichu. Statistikové z velkých souborů také přispěli svým dílem a k oddálení choroby doporučují pít kávu a brát vitamín B12. Také nikotin, kdyby to prý bylo korektní.
K čemu slouží chiméry?
Zatím se u parkinsoniků vědě daří jen mírnit projevy nemoci. Chiméry nás ale kvapně přibližují době razantnějších zákroků, které nemoc budou nejen brzdit, ale částečně i napravovat. Parkinson je zvláštní onemocnění tím, že nepostihuje všechny nervové buňky v mozku, ale jen ty, co mají v popisu práce produkovat dopamin. Když o ně přijdeme, nemáme kortikální kontrolu složitých pohybů a stává se z nás neohrabané dospělé mimino. Ač to tak nevypadá, tak řízení pohybu, se vším tím předvídáním, co se stane, pokud uděláme to či ono, je hodně složitá záležitost. Stačí se podívat na videa, jak se těm nejlepším programátorům a technikům daří stvořit chodící roboty.
U nás a nejen u nás to má na starosti lokalita zvaná bazální ganglia. Jsou součástí šedé hmoty koncového mozku. Kromě starosti o pohyb tu je také sídlo učení a vnímání strachu. Vývojově oblast patří mezi staré struktury. V případě japonských pokusů šlo o vstřikování lidských buněk opicím do místa zvaného putamen. Právě tam a v blízkém okolí je neuronů produkujících dopamin hodně třeba. Odtamtud se řídící signály k pohybu přenášejí do dalších částí mozku. Cestičky těmto spojům prošlapávají neurony využívající k domluvě dopamin. Když je ho nedostatek, třepou se nám ruce a někomu i brada.

Pokud budete mít někdy co do činění s vrávorajícím parkinsonikem, je dobré vědět, že i když to tak nevypadá, myšlení u těchto lidí být postiženo nemusí. Tím chci říci, že třesoucí se uzlíček neštěstí nás svou inteligencí často může lehce strčit do kapsy. Pochopitelně, že časem na parkinsonem postiženém mozku choroba přece jen vykoná své, včetně nevyhnutelné demence.
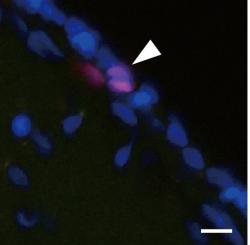
Za to, že se dnes Parkinsonu po delší době opět věnujeme, mohou slibné výsledky pokusů na opicích. Jde už o primáty a naše blízké příbuzné. V zemi vycházejícího slunce jim nejprve osvědčenou metodou Barry Kidstona zlikvidovali v mozcích dopaminergní neurony a udělali z nich těžké parkinsoniky. Pak jim nasadili léčbu iPS buňkami a tím jejich zdravotní stav do značné míry zase napravili.
CO jsou iPS buňky?
iPS, nebo-li induované pluripotentní buňky, jsou jedním z druhů kmenových buněk. A co jsou kmenové buňky? Kmenové, neboli SC (z anglického stem cells) jsou buňky, které nejsou ještě diferencovány v žádnou z konečných buněčných forem. Jsou to takové "čekatelky", které v našich tkáních jsou v klidu do doby, než je v poraněné a nebo opotřebované tkáni potřeba hasit průšvih a nějaký typ buněk rychle vyměnit. Kmenové buňky jsou tak trochu všeumělkyně s časově neomezenou schopností sebeobnovy a schopné se přeškolit do vysoce specializovaných buněčných typů. Kdo chce vypadat učeně, mluví o nich jako o buňkách pluripotentních.

Základní členění kmenových buněk je podle toho, odkud je odebereme. Je-li to z embrya ještě před jeho uhnízděním v děloze, pak se jim říká embryonální kmenové buňky. V odborné literatuře se už používá jen zkratka ESC. Pokud byl odběr proveden ze staršího zárodku, tedy až po implantaci embrya v děloze, pak se jim říká embryonální zárodečné buňky (EGC). Embryonální kmenové buňky lze získat ale i z ještě staršího zdroje - pupečníkové krve po porodu, případně z plodové vody. O těch se píše jako o buňkách AFC.

Pokud jde o "spící" kmenové buňky izolované z již dospělých a vyvinutých tkání, nesou označení ASC buňky.
Až teprve teď se dostáváme k indukovaným kmenovým buňkám , neboli iPSC. V jejich případě už nejde o "prvotní" kmenové buňky ale o buňky upravené ze somatických buněk. To znamená, že je vědci museli svými lektvary znásilnit, aby se z již hotových fibroblastů (buněk kůže) nebo z buněk krevních, posunuli v čase o krok zpět. Aby je znovu dostali do jejich školních let, kdy ještě nebyly specializované a byly buňkami kmenovými, a tak trochu jako teenageři zase byly buňkami "schopnými všeho".

I když jedno Čínské přísloví říká, že dvakrát nevstoupíš do téže řeky, u buněk to tak docela neplatí. Důkazem je i tento japonský pokus, o němž píšeme. Z lidských kožních buněk Takahashiho parta získala iPS buňky a z těch pak neurony.
Pochopitelně, že při tak krkolomné přeměně se vyskytly problémy. Z publikace se dozvíme, že opice "nespolupracovaly", jak se od nich očekávalo. Úspěšnost léčebného zákroku měla být úměrná počtu buněk, které příjemkyně dostaly. Jenže pravidlo - čím více, tím lépe, v tomto případě neplatilo. Ukázalo se, že důležitější než počet přenesených iPS buněk, je jejich "kvalita". Vědci hledali geny, které by jim mohly tyto rozdíly ozřejmit. Těch podezřelých, které vykazovaly různou míru exprese, měli jedenáct. V síti jim nakonec uvázl hlavní kandidát na úspěšnost transplantace - gen "jménem" Dlk1. Na ten prý bude potřeba dohlédnout v již plánovaných pokusech na lidech.
Co nám Japonci svou publikací sdělují?
1) Že lidské iPS buňky se v mozcích cítí jako doma. Dokonce i v těch opičích.
2) Že se v novém hostiteli adaptují, dávají vznik nedostatkovým neuronům a ochotně se ujímají syntézy místně nedostatkového zboží - dopaminu.
3) Že se k transplantaci vhodné iPS buňky dají získat jak z kůže, tak i z krve a že by mohlo jít o alternativu buněk připravovaných k obdobným léčebným zákrokům zatím jen ze středního mozku potracených lidských plodů.
Závěr
Japonská metoda by léčbu Parkinsona zlevnila a učinila ji dostupnější i pro nás "z podzámčí". Nemuseli bychom za ní jezdit až do Číny, neboť japonskou náhražkou za embryonální kmenové buňky by časem snad mělo jít léčit i v zemích, jako je EU, kde ve jménu morálky jsou plody považovány za lidské bytosti a ani v případě potratu jejich práva nesmí být dotčena a tudíž místo využití k léčbě nemocných putují do spaloven. Podle japonských vědců je terapie iPS buňkami v takovém stádiu připravenosti, že lze přikročit ke klinickým testům. S náborem pacientů pro tuto léčbu v Japonsku začnou v příštím roce.
Poznámka
Léčba spojená s transplantacemi pluripotentních buněk sebou nese jisté riziko vzniku rakoviny. To ale japonská studie nezmiňuje. Řada vědců je přesvědčena, že k eliminaci takového rizika není nic lepšího, než k transplantacím používat embryonální kmenové buňky. iPS buňky se jim proto jeví jen jako z nouze ctnost. Argumentují tím, že již jednou diferencované buňky, které vracíme v jejich vývoji o krok zpět, tak již řadu "klíčků" od svých původních schopností a dovedností zahodily. Míní tím přístupové kódy ke genům. Geny iPS buňkám zůstaly, ale se všemi už neumí pracovat. I když japonské pokusy nejsou zatím moc početné, obavy skeptiků nepotvrzují. S přeškolováním buněk by to tedy nemuselo být tak rizikové, jak se mnozí obávají. Stávající výsledky japonského týmu jsou v tomto směru více než optimistické. I když se za rok na lidech potvrdí, že mají pravdu, léčba kmenovými buňkami v EU přesto mít na růžích ustláno nebude, jak to ostatně dokládá kauza "Velký soud o malých buňkách".
Literatura
Tetsuhiro Kikuchi et al.: Human iPS cell-derived dopaminergic neurons function in a primate Parkinson's disease model, Nature (2017). DOI: 10.1038/nature23664
Kyoto University
Sonja Kriks et al.: Floor plate-derived dopamine neurons from hESCs efficiently engraft in animal models of PD, Nature. 2011 Dec 22; 480(7378): 547–551.doi: 10.1038/nature10648
DPH zvyšuje riziko demence
Autor: Josef Pazdera (28.01.2015)
Ztráta čichu jako předzvěst demence
Autor: Josef Pazdera (29.07.2016)
Navádí Parkinsona vagus?
Autor: Josef Pazdera (02.05.2017)
Klotho by nás mohla zachovat fit a mysli otevřené
Autor: Josef Pazdera (12.08.2017)
Diskuze: