Rostliny dělají fotosyntézu tak, že spotřebují oxid uhličitý, využijí světelné záření a vyrobí organické látky, tedy cukr a pak ještě vodu s kyslíkem. Tohle je fajn a jistě by bylo užitečné se takový trik od rostlin pořádně naučit. S fotosyntézou si ale také můžeme hrát a zkoušet ji různě upravit nebo vylepšit. Pustil se do toho i chemik Fernando Uribe-Romo z Univerzity Centrální Floridy (UCF) s týmem studentů. A podle všeho úspěšně.
Povedlo se jim spustit proces podobný fotosyntéze v důmyslně vytvořeném syntetickém materiálu, kterým mohou zpracovat skleníkový plyn v atmosféře a přitom vyrobit energii. Takový proces má veliký potenciál pro vývoj technologií, které mohou významně omezit skleníkové plyny a ještě přidají příjemný bonus v podobě energie. Podle Uribe-Roma je to průlom. Po odborné stránce to prý bylo dost obtížné, ale aplikace by mohly být velmi zajímavé.
Když se poslední dobou objeví podobné zprávy o téměř neuvěřitelných chemických reakcích, odporujících běžné zkušenosti, tak můžeme docela dobře očekávat, že v tom budou namočené kovové organické kostry, čili koordinační polymery známé jako MOF (podle anglického Metal-Organic Framework). Uribo-Romo a spol. vyrobili jeden takový MOF a spustili v něm chemickou reakci, která přemění oxid uhličitý ze vzduchu na organické látky, které je možné zpracovat jako palivo.
Vědci se o něco podobného snaží už dlouhé roky. Zásadní problém byl v tom, jak zařídit, aby záření z oblasti viditelného světla spustilo požadovanou chemickou reakci. Pro ultrafialové záření, které nese hodně energie, není zase takový problém rozjet reakci tohoto druhu v běžném materiálu, jako je například oxid titaničitý. Jenomže ultrafialové záření představuje jenom asi 4 procenta záření, které dostává Země od Slunce. Velkou většinu slunečního záření tvoří právě viditelné světlo, tedy záření od fialových vlnových délek až po červené. Ale najít vhodný materiál, který by umožnil požadovanou reakci za působení viditelného světla, zase není vůbec snadné.
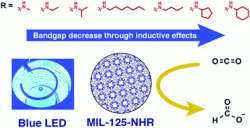
Badatelé vyzkoušeli leccos. Jen si ale potvrdili, že sice existují nějaké takové materiály, jsou ale vesměs vzácné a také pořádně drahé. Nákladná technologie s platinou, rheniem nebo iridiem by se uplatňovala jen těžko. Tak přišla řada na kovové organické kostry. Uribe-Romo a jeho tým vyvinuli MOF z titanu, tedy běžného netoxického kovu, k němuž přidali organické molekuly N-alkyl-2-aminotereftalátů. Tyto organické molekuly v MOF fungují jako světlosběrné antény. Mohou být navrženy tak, aby absorbovaly viditelné záření o určité vlnové délce – v tomto případě modré světlo.
Uribo-Romo a a jeho kolegové uspěli a MOF pěkně přetváří atmosférický oxid uhličitý na dvě redukované formy uhlíku – formiáty čili mravenčany a formamidy. Teď je čeká další vylepšování a zvyšování výtěžku této reakce. Také chtějí zkoušet další vlnové délky viditelného světla a hledat další podobné MOFy. Výsledkem jejich snažení by mohly být stanice na lapání a přeměnu CO2, které by stály u každé elektrárny či továrny vypouštějící oxid uhličitý. Zneškodnily by skleníkový plyn a ještě by dodávaly energii. A podobné materiály by vlastně mohly být leckde, třeba na střechách domů. Odstraňovaly by oxid uhličitý a zásobovaly by dům energií. Bude to chtít nové technologie a infrastrukturu, ale podle Uribo-Roma to už je v zásadě možné.
Video: Fernando Uribe-Romo on Synthetic Photosynthesis
Literatura
University of Central Florida 24. 4. 2017, Journal of Materials Chemistry A 7. 4. 2017.
Hacknutí fotosyntézy pro záchranu lidstva
Autor: Stanislav Mihulka (27.09.2014)
Průlomový solární článek vyrábí palivo z oxidu uhličitého a slunečního záření
Autor: Stanislav Mihulka (02.08.2016)
Zázrak jménem MOF: Zařízení na solární pohon vyždímá vodu ze vzduchu
Autor: Stanislav Mihulka (19.04.2017)
Diskuze:
Jak sežrat pomocí energie skleníkový plyn a konopí.
Josef Hrncirik,2017-05-28 16:49:44
Kvůli neočekávaně velkému zájmu pěstitelů o toto navýsost logické i ekologické téma se pokusím ukázat na nepřekročitelné mantinely fotosyntézy, přestože o ní prakticky nic nevím a proto mohu pokračovat rychle a snad přehledně.
Teoreticky elektrolýza vody vyžaduje rozkladné napětí jen cca 1,2 V,
tj. energii 2*1,2 = 2,4 eV/ molekulu vody, technicky se počítá s napětím 1,5 V zejména kvůli přepětí kyslíku i na Pt elektrodách.
Elektrolýza CO2 na uhlan a vodan žádá cca 5,2 eV; 1,3 V napětí teoreticky je nepříznivější oproti 1,2 V teoretickým pro vodu.
2,4 eV pro vodu by mohl dodat foton 415 nm. Těch je však ve spektru málo, voda je neabsorbuje a disociací vody nutně vzniklé přechodné meziprodukty by vyžadovaly větší energii, tj. kratší vlnovou délku a navíc by takové záření rychle bílilo či oxidovalo organické látky, zejména fotoaktivní.
Ideální je rozdělit reakce i energii na poloviny (a prostorově je oddělit, i vzniklé redukovadlo a oxidovadlo co nejlépe odělit, než Vás oddělají prudkou reakcí)
Polovinu energie dát při redukci a polovinu při oxidaci, tj. 1,2 eV při vyredukování 1 molekuly H2 a 1,2 eV při vyoxidování 1/2 O2.
Potom sice potřebuji 2x tolik fotonů, ale více dostupných (až po 830 nm) a ochočenějších.
K vyredukování potenciálně 1 atomu do molekuly H2 by pak postačila vlnová délka pod 1630 nm. To je příznivá stránka náhrady 1 fotonového brutálního mechanizmu sofistikovanými následnými ději (4 f/ 1 H2O).
Rozumné uvolnění O2 probíhá asi jako 4 e děj.
Bylo by možno postupovat i jen s 1 e. H2O; OH- není redox!!;; OH- -e = OH* (brutálně oxidační radikál)!; dál už to je nuda. 2 OH* = H2O2; 2H2O = 2 H2O + O2. Možné problémy kinetiky 4 e děje řeší děj 1 e, ale má velký energetiký nárok a produkt ničí okolí.
Při fotoaktivaci vzniká v anténě elektron a díra, tj. redukující oblast a oxidující oblast. Aby zlomyslně nerekombinovaly, redukující část musí dříve zreagovat s nějakým užitečným oxidovadlem a podobně oxidující část musí zreagovat s užitečným redukovadlem.
Vyredukovat z vody (či tím spíše z organického katalytického meziproduktu) H2 je relativně jednoduché.
Fotoaktivací ze středně silného redukovadla Rd vznikne silné redukovadlo RD redukcí nebo spolu se slabým redukovadlem rd disproporcionací.
Protože organické redukce probíhají většinou jako 2 e děj píši raději sichrově úhrnně:
2 rd + 2f + 2e = 2Rd
2 Rd + 2e + 2f = 2RD
2 RD + H2O = H2 + 2OH- + 2 Rd ; (ev. i nechtěné H2)
nebo chtěná fixace CO2
2 RD + CO2 + H2O = HCOO- + 2 OH- + 2 Rd a konečně sladké
2 RD + HCOO- + 2 H2O = CH2O + 3 OH- + 2 Rd
Absorbce f udržuje nutnou vysokou hladinu RD ať již vznikají čerpáním redukcí či nepravděpodobnou disproporcionací 2 Rd = RD + rd formálně bez nutnosti zápisu e. I zde však nutně s probíhající redukcí musí být někde svázána oxidace, elektrony se jen přesunují, nemizí ani nevznikají.
Vše se to dá chápat i jen jako následné fotolýzy.
Ptoto je nutno se vždy ptát i na opačný děj, na oxidaci.
Proto jsem se vždy ptal, kde mizí kyslík.
Zda jej nespaluje v koncentrátoru nenápadně v noci chlorofyl, metylkyanid, TEOA či žid- le?
Oxidační cesta je vždy riskantní a lehce se zvrhává. Je však stejně nutná a nevyhnutelná jako redukce.
Zcela analogicky je to v oxidační větvi, na jiném specializovaném fotokatalyzátoru.
Slabé oxidovadlo ox + 2f -2e = 2 Ox se fotooxiduje na střední (či již postačující) Ox až po jistě postačující SILNÉ OX
2 Ox + 2 f - 2e = 2 OX
Máme-li štěstí, extrémně silné OX se pak rozloží na O2 bez výbuchu (na rozdíl od acetonperoxidu či konc. H2O2) či i jen vybělení okolí a možno machrovat, že jsem formálně v úhrnu bilancí naoxidoval vodu (jakoby na anodě).
4 OX + 2 H2O = O2 + 4H+ + 4 Ox
Foto LÝZA či syntéza?
CO2 + H2O = CH2O + O2 ;+4e;-4e; ?nejspíše 4 + 4 = 8 f; 8*0,65 eV min tj. min. 1535 nm
To jsou asi nepřekročitelné mantinely. Jak to je ve skutečnosti vůbec netuším, nemaje hnojárnu.
Možná stačí i jen jednostupňové redukce i oxidace ev. dobrá díra v dobré kostře a poblíž ukázněně na povel vyčkávající e.
Re: Jak sežrat pomocí energie skleníkový plyn a konopí.
Josef Hrncirik,2017-05-28 21:00:42
Nelze jen redukovat nebo oxidovat.
Redukční a oxidační řady, přestože mají různé anténní systémy a koncovky řad reakcí mají v naprosto rozdílné oblasti redox potenciálů, jsou nutně spřaženy v oblasti blízkých redox potenciálů nějakými společnými (nenápadnými) slaboučkými commonred a commonox, které tak uzavírají obvod fotoelektrolýzy.
Ta se pak bilančně jeví jako fotodisociace vody či CO2 zbytečně velkým počtem fotonů, což však umožňuje uskutečnit reakci bezpečnějším mechanizmem a dostupnějšími fotony. Aby se uložilo velké množství využitelné energie je bezpodmínečně nutné uvolňovat i volný kyslík.
Nelze si pomáhat jeho předčasným spalováním pomocí Spasitele (Sacrifacing Agent) ať již TEOA či jinými obětinami.
Reakce potom sice táhnou požadovaným směrem, ale rozhodně se žádná podstatná energie neakumuluje, li vůbec jaká.
Ani formální kvantovou účinnost požadované fotolýzy CO2 to i se Spasitelem nemělo nikdy úhrnně větší než 10**-4.
Taková je smutná pravda o anténách, spřažených dějích, užitečné reaktivitě a fotostabilitě.
Prečo si smedný dromedár lebo ťava neurobí vodu treba aj bez kyslíka ako rastliny?
Josef Hrncirik,2017-05-26 16:35:36
Viz tento Osel, již v 1. větě?
Kovové kostry určitě nevyrobily m.c.c, alebrž ji spotřebovaly!
Josef Hrncirik,2017-05-14 11:25:59
V nejlepším případě odebraly exergii mimosmluvně a bez platby z jističů.
Josef Hrncirik,2017-05-14 11:44:56
Modré světlo žere mozek
Josef Hrncirik,2017-05-14 16:13:35
Fotometrický, spektroskopický, chemický i energetický horor, vše v 1.
Ampulky obsahovaly cca 1,5 ml suspenze s cca 4 mg MOF kostlivců.
Tvrdili, že tok fotonů cca 2 eV je cca 1,9 mmol/L.h.
Při trvání 120 hod ampulkou prošlo cca 1,9*1,5*2*120*10**-3-3+5 = 68 000 A*V*s = 68 kJ.
Chybí odhad hodnoty W/cm2 snad cca 0,12 W/cm2 modré složky, pochopitelně raději přeměřený, avšak dobře odpovídající cca 0,1 W /cm2 modré složky u země.
Posoudit však, zda se to světlo dostatečně absorbovalo nelze, v práci nikde není hodnota absorbance s koncentrací či hotového extinkčního koeficientu.
U obr. 4a na s. 17 a či na s. 6 se píše o integrační kouli, ale navážka je tajná a absorbance je bez hodnot i v supplements S65.
Na s.7 sice laškovně píší, že 3 cm suspenze v metylkyanidu měly absorbanci cca 0,2; koncentrace je též zase tajná.
Nezbývá než věřit, že listí je dostatečně statečně červené.
Z obr. 3 na s.14 je vidět, že to museli sytit čistým CO2, protože 4 mg kostlivce by nasorbovaly ze vzduchu jen max. cca 0,08 mg CO2.
Tento humor žertovně nabízejí za více než 40 liber, supplements zdarma.
Díky Voloďovi se to však dá stáhnout celé zdarma na proruském scihub webu hubícím scifake pod DOI = 10.1039/c7ta00437k
Je to stejný nesmysl jako Osel 18.III.2017 17.56 Důmyslná molekula žere CO2 jako divá
Josef Hrncirik,2017-05-14 17:11:50
Jak vidno zříti na 10.1016/j.crci.2015.11.026
"Obětováním elektronového donoru v záři slunečního koncentráku lze úspěšně simulovat výrobu solárního paliva".
Fotosyntéza zvládla přípravu elektronů pro redukci CO2 fotooxidací vody.
Tím též připravila kyslík nutný pro dýchání.
Tento majstrštyk se zatím alchymystikům nedaří a proto studují fotoredukci s elektrony buď z drátů, nebo alespoň z pomocných látek, které je sice dodají, ale přitom se nutně naoxidují (vlastně ZHOŘÍ).
Nejlehčí je vyrobit vodík na úkor stejného množství obětovaného, tj. 0 od 0 pojde, pokud k 0 ztrátě dojde (nikdy nedojde!).
Pro své hokusy nejraději používají trietanolamin TEOA, protože podobně jako peníze nesmrdí, na rozdíl od účinnějšího, avšak páchnoucího trietylaminu TEA, smrdícího více než práce.
Odevzdáním (loupeží, obětováním) elektronu z TEOA vznikne TEOH+ a reaktivní radikál poskytující další elektron a H+ iont (sumárně vlastně H atom) a rozpadávající se na dietanolamin a hydroxyacetaldehyd, které se mohou též podobně dále oxidovat.
Proto je nutno ptát se, kde mizí kyslík z CO2.
Na jedné straně (pod kotlem) spalujeme TEOA a ve svíčce si pak naloupenými elektrony pracně redukujeme trochu CO2 třeba i z oxidace TEOA.
Trhy to chtějí a tak to nemá chybu.
Přiložte pod kotle, doba to žádá!!!
Dejte si na střechu 40 g kovových kostlivců/m2
Josef Hrncirik,2017-05-14 18:23:50
suspendovaných v cca 10 kg metylkyanidu.
Po 100 letních dnech sklidíte dle S59 0,014 mol/L*13 L/m2 = 0,18 mol oxidu uhelnatého zabudovaného do formiátů vzniklých reakcí s TEOA.
Modré je totiž ve spektru 10x méně, než NATO svítili.
U "modré žere mozek..." jsem si naivně myslel že jen o 10 dB neklamou.
Zabudovalo se cca 0,018*2*1,5*100000 J = 54 kJ.
Spotřebovalo se však 0,1*10000*3600*120 = 432 MJ.
Účinnost akumulace je tedy max. 0,013%, podobně jako u pažravé divé molekuly.
TAKOVÁ JE ZHRUBA I QUANTOVÁ ÚČINNOST.
Jimi uváděných cca 1,8% je tedy obvyklá klamavá reklama 30 dB.
Jen 5% získaného formiátu je jako sůl, 55% je hydroxyetylaminformiát,
45% dihydroxyetylaminformiát.
Příjemné oddělání od metylkyanidu a TEOA a regeneraci ve slunečním koncentráku přeji.
Pomlčel jsem o dalších oxidačních produktech TEOA a nutném zmýdelnění formamidů před ev. využitím formiátů.
Určitě je nejlepší vše po zakoupení okamžitě spálit v peci koncentráku (slunného koncentrátoru).
Po 10 dnech opalování se kostrouni na střeše obrátí max. 1x (S1 turnover number i jen 0,2).
Jak vidno z S59 bez TEOA ani ránu. Bez něj formiáty nevznikají, avšak fotorozklad kostrounů s TiO2 vznikajícího v a z MOF vede na cca 10% (vůči CO2) formiátů i bez CO2 a 1% vzniká i potmě.
Zdá se, že kostrouni se nebudou schopni otočit na střeše ani 100x.
Do pece s nimi!
Sorry jako (Vole). DARPA Jim skočí na lepší špek.
Josef Hrncirik,2017-05-15 07:15:41
3 CO2 (greenhouse) = (C3 (cracene) + 2 O3 (metallic); MOAB)
Re: Sorry jako (Vole). DARPA Jim skočí na lepší špek.
Josef Hrncirik,2017-05-15 09:52:57
Pro prudké uvolnění velkého množství energie v MOAB je nutno vzájemně zredukovat silné oxidovadlo a zoxidovat silné redukovadlo (spálit silné palivo tj. současně "spálit palivem silné oxidovadlo").
Při akumulaci energie je nutno z popela zpět připravit ("vydělit") palivo a oxidovadlo.
Fotosyntéza prostě fotolýzou z vody uvolní O2 (oxidovadlo) a jednoduše "zbyde" palivo
2 H2 (redukovadlo).
Do 18 g vody tak uloží 2 moly*cca 1,5 elektronvoltů = cca 300 kJ energie.
Protože vodík nelze rozumně skladovat, je dál energie převedena do vazeb C-C či C-H.
V podstatě reakcemi 2 H2 + CO2 = -(CH2O)- + H2O kde úbytek energie je zanedbatelný, avšak oněch cca 2*300 kJ je uloženo do 30 g CH2O + 32 g O2, tj. 31 g/ca 300 kJ.
Klamavou reklamou lze však tvrdit, že místo 2 g H2 potřebuji 32 g CH2O či 7 g = (CH2)/2 vždy cca na 300 kJ (pokud beru O2 přímo z atmosféry).
Pokud se však jen přeskupují vazby mezi -O- a -C- či -H a nevzniknou vazby O-O ať již v O2 či alespoň v H2O2, podstatné množství energie se neakumuluje či při hoření neuvolní.
Při anaerobním přesmyku glukozy na kyselinu mléčnou se uvolní jen cca 1/10 energie než při jejich oxidaci.
Příprava formiátů z TEOA fotolýzou probíhající bez uvolnění O2 není schopna akumulovat významné množství (navíc snadno uvolnitelné energie).
Možná se dokonce energie "ztrácí".
Určitě se však znečisťuje a mizí TEOA, v tomto podivném systému nutný.
To si zrovna můžeme přímo pálit TEOA či jiné látky pod kotlem či v palivovém článku, leč bez článků a grantů.
Re: Re: Sorry jako (Vole). DARPA Jim skočí na lepší špek.
Josef Hrncirik,2017-05-15 15:14:58
Šotku nezlob!
Všelikým kvaltem se tam dostalo občas místo formamidů formiátů.
V energetickém rámci 2 molů e- při zhruba stejném napětí pak
2 g H2 odpovídá cca 15 g cukru či cca 5 g uhlovodíku CH2 či jen 4 g metanu či 6 g uhlíku a 7 g Li při jeho 3 V.
Re: Je to stejný nesmysl jako Osel 18.III.2017 17.56 Důmyslná molekula žere CO2 jako divá
Florian Stanislav,2017-05-16 22:01:25
Píšete : "Fotosyntéza zvládla přípravu elektronů pro redukci CO2 fotooxidací vody."
No nevím, že by se voda dala oxidovat, když sama je konečným stupněm oxidace vodíku. Fotosyntéza začíná fotolýzou vody, vznikají redukvané složky s vázaným vodíkem, pak následuje fixace CO2 a vznik glokosy.
1. Na redukci 44 g CO2 na CO je třeba dodat 285 kJ, tedy 6 478 J na 1 g CO2. Spálením CO na 44 g CO2 vznikne 285 kJ.
2. ČR produkuje asi 12 tun CO2/obyvatele (1,2E+7 g CO2 /obyv), celá ČR při asi 10,5 mil obyv. spotřebuje při redukci CO2 na CO energii 6478 J na 1 g CO2, celkem 1,2E+7*1,05E+7*6478 =8,16E+17 J /rok.
Na 1 m2 ČR dopadá asi 1000 kWh sluneční energie za rok. 1 kWh = 3,6E+6 J, tedy 1000*3,6E+6 =3,6E+9 J/m2 =3,6E+15 J/km2. Při účinnosti 1% umělé fotosyntézy kombinované s výrobou elektřiny to bude
3,6E+13 J/km2.
Potřebujeme tedy (8,16E+17)/(3,6E+13) = 22 700 km2, což je čtverec asi o straně 150 km.
Při účinnosti 10% to bude 2 270 km2, čili čtverec o straně asi 47 km.
Re: Re: Je to stejný nesmysl jako Osel 18.III.2017 17.56 Důmyslná molekula žere CO2 jako divá
Josef Hrncirik,2017-05-17 07:40:38
Po rozetnutí gordického uzlu vody, je nutno jej znovu slepit škrobovým lepidlem Drago, nebo alespoň škrobovým hydrolyzátem či jinými Éčky či alespoň javorovým sirobem.
Jinak nám neposedný H2 zahne roha.
K fotolýze vody teoreticky stačí dle tabulek Gibbsovy exergie cca 1.2 e.V, tj. cca světlo 833 nm.
Při elektrolýze je technicky nutno cca 1,5 V oproti teorii cca 1,2 V, pak by stačila velmi podezřelá vlnová délka 666,666 nm spojené rudé čínsko-sovětské vlajky PRCCCCP.
To by možná řešilo nutné vyšší energie aktivovaných stavů a tím potřebnou kinetiku.
Stále však zůstává problém jak zabránit okamžitému zpětnému spálení "nažhavených a nasvícených silně nekompromisních aktivovaných radikálů" a jak zabránit úniku neposedného H2 po rozbití molekuly vody úderem bucharu.
To lze provést tak, že na jednom skřipci molekuly vody (či jiné látky (CO2)...) redukujeme (méně elektronový problém s menšími "přepětími") a na druhém skřipci s nutným waterboardingem či raději metylcyanideboardingem molekuly vody (či jiné látky (obětovaného Spasitele TEOA ...) oxidujeme.
Oxidaci a redukci je vhodné prostorově hodně oddělit, aby nedošlo ke zpětné reakci (zkratu, propalu) jako u Hindenburka.
Protože náboje nelze před bojem příliš nahromadit, redukce a oxidace probíhají globálně současně a dají se chápat jako prostý rozklad -lýza.
Každý dostane co chce.
Oxidací vody na anodě dostanu podle podmínek OH*; O3; O3-; O2; O2--; H2O2. Pochopitelně nejsnáze (ale s nepřijatelným přepětím) získám O2.
Proto O2 pálí C při výrobě Al, nebo Spasitelem TEOA při prodeji divých pažravých molekulárních kovových kostlivců.
I když jsou utopení v metylkyanidu, aby tam přednostně nevznikal neposeda H2, stejně z části vzniká a když se jim systém naoxiduje a zčásti rozsype vzniká ještě snadněji, navíc jim to vlhne víc něž prach.
Katoda = s Pt nuda.
Čtverce nad odvěsnami je zatím předčasné vyměřovat.
Eko
Alexandr Kostka,2017-05-14 10:51:01
A) neskutečné, kolik vedců se snaží přiživit na dávno vyvráceném podvodu s globálním oteplováním a "problému" CO2.
B) "Eko" fabrika je nesmysl, jediná která je ekologická je ta, kterou nepostavili. Stojící továrna, která úmyslně vyrábí výrobky se zkrácenou dobou životnosti, lecdy zcela zbytečné a poměrně často takové, které místo byť jediného použití nějakou dobu zaberou místo ve skladu (či v domácnosti) a pak zamíří na recyklaci JE ekologická katastrofa, bez ohledu na to, kolik "zelených" technologií tam někdo nacpe. Primárně není potřeba takové "výrobky" vyrábět "zeleně", ani recyklovat, ale vůbec je nevyrobit, nepřevážet tisíce kilometrů, nevyhazovat je atd.
C) Ovšem coby zvýšení účinnosti elektrárny, případně že by si továrna část enegrie vyrobila sama je to plus.
Re: Eko
Jiří Novák,2017-05-14 19:46:01
Tleskám. Teď ještě přesvědčit firmy, aby místo šmejdů na jedno použití vyráběly trvanlivé a především snadno opravitelné výrobky.
Re: Eko
Libor Tomáš,2017-05-14 22:32:15
Bohuzel mate pravdu. Navic mnozstvi CO2 je nejnizsi v cele historii zeme (vetsina skoncila ve vapencich a cast v uhli a rope). Mit ho min, tak uz tady nic neroste. Skutecny problem je tedy jak vyprodukovat co nejvic CO2, aby se rostlinam lepe rostlo, pouste byly mensi a planeta zelenejsi.
Rovnez je treba bojovat proti dobe ledove, ktera muze prijit kdykoliv. Radeji pestovat pomerance nez mit pod nohama kilometr ledu.
Re: Re: Eko
Alexandr Kostka,2017-05-15 01:12:41
CO2 nemusíme ani extra produkovat, ani extra spotřebovávat. Jednak je lidský příspěvek k jeho množství v atmosféře zanedbatelný, dvak je tam rovnovážný vztah. Méně Co2, méně rostlin. Více Co2, více a rychleji rostoucích rostlin. Potíž je spíš v nesmyslném plýtvání nenahraditelnými surovinami. Kolik let se ví, že uhlí, ropa a plyn jsou mnohem lépe využitelné, než aby jen tak shořely? Kolik let máme náhradu ve formě jaderných elektráren? Jak to dopadlo? V "civilizovanější" části světa ůzelení" jádro zakázali, a místo toho budují větrníky a soláry a uhelné či plynové elektrárny hoří dál. Ovšemk naprázdno, jen jako záloha za tyto nespolehlivé zdroje. Kovy? Totéž. Vytěží se, něco se vyrobí a pak to (v nejlepším případě po nějaké době používání) skončí na sklásdce. V takové směsi, že to z ní prakticky nejde extrahovat. Příroda si sice za pár (set) tisíc let poradí, kovy z toho voda vylouhuje a spláchne do nějaké prolákliny, ale to už nám jako lidstvu může být jedno. Počítám, že naši potomci jednou budou dnešní dobu popisovat jako zcela šílenou a absolutně nezodpovědnou.
Re: Re: Eko
Roman Sobotka,2017-05-15 10:18:33
Jednou za cas to tu opakuji.... vice CO2 nemuze mit na realnou produkci biomasy fototrofu (rostliny, rasy, sinice) zadny podstatny efekt. Rust je v drtive vetsine biotopu limitovan mnoha jinymi faktory, jako je mnozstvi dusiku a fosforu, zeleza (oceany), vody atd atd. Prihnojenim CO2 se v prirode nic nezmeni, pokud nedodate vse ostatni, co rust limituje. Rostliny porostou na 200ppm CO2, nic zasadniho to neznamena. Pri vyssim CO2 pouste urcite nebudou mensi, spise vetsi diky vyssimu odparu. Chapu, ze nekdo nema rad environmentalisty, ale to jeste neznamena ignorovat zakladni fakta.
Re: Re: Re: Eko
Libor Tomáš,2017-05-15 14:21:22
Muj vztah k enviromentalistum, ekologum a klimatologum je neutralni. Sam jsem kdysi ekologii na VS absolvoval. Co lidi nemaji radi jsou ruzni aktivisti a politici, kteri tyto obory poskozuji a zneuzivaji k dojeni rozpoctu, budovani politicke kariery a pachani dobra.
Mnozstvi CO2 kazdopadne vliv ma. Na ziskani nejake ziviny musi rostlina vynalozit urcitou energii. Napr. pokud je voda hluboko tak potrebuje dlouhy koren, ktery neni zadarmo. Pokud je koncentrace CO2 nizka, tak rostlina musi mit dele otevrene pruduchy, aby ziskala pozadovane mnozstvi a to znamena i vyssi odpar vody. Takze vic CO2 znamena, ze rostliny mohou rust i v nekterych poustnich oblastech kde to momentalne neni mozne. Afaik tady byl kdysi clanek na toto tema.
V tom, ze rostliny nepotrebuji jen CO2 mate pravdu, ale pokud zlepsite jeho dostupnost tak mohou usetrene zdroje pouzit na ziskani jinych, hure dostupnych latek a porostou lepe. Samozrejme v ramci nejakych rozumnych hranic.
Nicmene kdyz se podivame na historii zeme tak dnes zijeme v obdobi, ktere je hodne studene, suche a s nizkou koncentraci CO2. V kambriu bylo 16% CO2 ve vzduchu, pak klesalo na 10% v karbonu, 1% v permu, vyssi bylo az v kride - 6% a postupne kleslo na dnesnich 0,04%
Re: Re: Re: Eko
Alexandr Kostka,2017-05-15 19:42:05
Ano, krásně jste vysvětlil, proč to NEMÁ vliv. Ovšem vaše vysvětlení má jeden jediný drobný nedostateček: V pokusném skleníku, kde je vše stejné, jen CO2 je víc to prostě MÁ. vliv. A tio obrovský. Rostliny jsou viditelně silnější a rostou lépe, rychleji, mají tudíž podstatně silnější kořeny, schopné čerpat víc živin (a to i v chudé půdě) atd. PS: a tuším ještě mnohem větší efekt to má na přírůstek biomasy v planktonu.
Re: Re: Re: Re: Eko
Roman Sobotka,2017-05-15 22:25:28
Ja bych rad byl takovy optimista, ale skepse je proste na miste. Polnich pokusu s vysokym CO2 se delalo a dela mnoho. Klasicke optimisticke review, kde se resi pozitivni vliv na vodni rezim, koreny atd je treba toto (pro zajemnce):
https://www.ars.usda.gov/ARSUserFiles/60100500/csr/ResearchPubs/prior/prior_11a.pdf
Uz z toho je ale videt, ze i tak uplne velky zazrak to neni. C4 rostliny rychleji prilis nerostou ani za idealni podminek, C3 rostliny idealne ano, ale casto se pouzivaji koncentrace CO2 750ppm, 1000ppm (tedy hodne vysoke). Podle jinych praci muze byt realny dopad CO2 kolem 500ppm dost mizerny, prevazi ostatni vlivy jako je limitace vsim moznym (kde nic neni, ani delsi koreny nepomohou), fotoinhibice, pocasi... kdo si troufne tvrdit, jake bude podnebi pri 750 ppm CO2?
Dalsi problem je nutricni kvalita, ktera jde u CO2 hnojenych rostlin dolu. Vice redukovaneho uhliku, ale malo mineralu. Napr:
https://www.nature.com/nature/journal/v510/n7503/full/nature13179.html
https://elifesciences.org/content/3/e02245
Re: Re: Re: Re: Re: Eko
Alexandr Kostka,2017-05-17 18:23:39
První článek jsem pročítal docela pečlivě, ale o "minimálním" efektu vyššího CO2 se tam opravdu nikde nepíše. Říkají tam, že s vyšším podílem CO2 v atmosféře obrovsky roste efektinost využití vody. Konkrétně tvrdí, že u C3 je skoro dvojnásobná, a u C4 je rozsíl menší, bez čísla. Čímž je to vysvětleno, u většiny jen tak divoce rostoucích rostlin jaksi JE limitujícím faktorem množství vody k dispozici, potažmo jak efektivně tu vodu umí využít. To o živinách jsem netušil, díky za info. A celkově díky za velmi přínosné odkazy, rád jsem početl.
Teda pane Mihulka, to jsou naprosto
Josef Blecha,2017-05-14 10:43:22
nové objevy, že rostliny fotosyntézou "vyrobí organické látky, tedy cukr a pak ještě vodu s kyslíkem". V učebnicích se sice píše a experimenty to potvrzují, že při fotosyntéze vzniká z vody kyslík, ale třeba se učebnice mýlí a rostliny tu vodu i kyslík skutečně vyrábějí, otázka je jenom z čeho? Kde jste se toho dopídil?
CO2
Karel Ing. křivan,2017-05-14 10:19:45
Což zvýšit jeho obsah ve sklenících ? Je to přece "potrava" pro rostliny ? Spíš něco jako "zaplynované pařeniště".
Re: CO2
Alexandr Kostka,2017-05-14 11:01:17
Nápad dobrý, ale jak to chcete udělat? I ty nejčistší zplodiny obsahují kromě CO2 i dost fuj věci. Když je budete pouštět na rostliny "jen tak", tak možná některé druhy vyrostou a budou prosperovat, ale získáte tuny lehce zamořené biomasy, se kterou by se mělo zacházet jako s nebezpečným odpadem. Asi by šlo udělat nějaké nanosítko, kterým by procházela maximálně molekula velikosti CO2, ale protlačovat něčím takovým veškeré zplodiny byť ze středně "menšího" podniku by bylo energeticky velice náročné. Jde o obrovské objemy a navíc potřebujete, aby "odtah" nekladl odpor.
Opravdu dva ze dvou?
Adam Trhoň,2017-05-14 01:04:58
Dejme tomu, že pořídím střechu z tohoto materiálu. Střecha bude pohlcovat skleníkové plyny a produkovat palivo. Abych získal energii, palivo musím spálit, čímž skleníkové plyny vrátím do atmosféry. Chápu něco špatně?
Re: Opravdu dva ze dvou?
Stanislav Kaderabek,2017-05-14 02:30:53
Budete mit timto natrene steny kotelny a odstranite komin, zadny problem...
Re: Opravdu dva ze dvou?
Jan Novák9,2017-05-14 05:49:46
CO2 není problém sám o sobě, oceán je schopný ho všechen pohltit, jenom voda se promíchá až za asi 1000 let. Můžete palivo využít k tomu že další palivo vynesete na Titan :-)
Jako likvidace CO2 je to podobné jako plány na zachycení CO2 s CaO + CO2 > CaCO3, s tím že ten CO2 se musel před tím uvolnit z vápence vypálením.
I kdyby to využilo jenom 4% slunečního záření, bude to mnohem účinnější než fotosyntéza.
Diskuze je otevřená pouze 7dní od zvěřejnění příspěvku nebo na povolení redakce