iRNA bude léčit
Ne, v titulku tentokrát není překlep. Léčit nebude nějaká Irena, ale iRNA čili „ribonucleic acid interference”. Do medicíny rázně vkročila nová odnož molekulární genetiky.
Zástupci americké soukromé biotechnologické společnosti Acuity Pharmaceuticals oznámili, že jako první na světě provedou klinické testy léčby založené na principu tzv. RNA interference (iRNA). Cílem léčby se stanou degenerativní změny sítnice, které poškozují zrak mnoha lidem v pokročilejším věku a u některých mohou dokonce způsobit trvalou ztrátu zraku.
RNA interference není lidským vynálezem. Jako obvykle jsme ji „ošlehli“ z přírody. Je nastartována přítomností dvojšroubovicové molekuly RNA. Tento proces se zřejmě vyvinul jako ochranný mechanismus proti virům vybaveným dědičnou informací v podobě dvojité šroubovice RNA. Buňky se naučily ničit mRNA, která odpovídá pořadím písmen genetického kódu této dvojité šroubovici RNA a nadobro tak vypnou produkci bílkovin, která se podle této mRNA v buňce vyráběla. Je jasné, že tak je zabráněno viru v tom, aby si nechal buňkou vyrábět své bílkoviny. Jak už to v přírodě chodí, naučila se buňka mechanismu využít i pro jiné účely, např. pro regulaci genů. Taková vlastní dvojitá šroubovice RNA působí jako účinná brzda genu a přitom nepůsobí na úrovni DNA. Gen ať si klidně dělá co chce, RNA interference zabrání tomu, aby buňka pocítila důsledky „práce“ tohoto genu. Pokud bychom si dění v buňce rozdělili na tři patra: gen – RNA – bílkovina, pak RNA interference reguluje dění v buňce na úrovni „druhého patra“.
RNA interference se ukázala jako účinný „vypínač“ genů v mnoha pokusech, z nichž první proběhly na modelovém červu Caenorhabditis elegans koncem devadesátých let 20. století. Jasně se prokázalo, že dokáže úžasné kousky i v lidských buňkách. Nyní tedy aspiruje na praktické uplatnění.
Degenerace sítnice je vyvolána nadměrným růstem krevních kapilár, které mají křehké stěny, praskají a krev, která se z nich vylévá, pak ničí světločivné buňky. Za růst krevních kapilár může zvýšená produkce růstového faktoru VEGF. V Acuity Pharmaceuticals vyvinuli krátkou dvojšroubovici RNA (tzv. siRNA čili small interfering RNA – česky „malá interferující RNA“ ) označovanou kódem Cand5. Tato siRNA má pořadí „písmen“ genetického kódu shodnou s částí mRNA, podle které se v buňkách tvoří růstový faktor VEGF. Měla by proto zajistit rozložení mRNA pro VEGF a tím vlastně příslušný gen „vypnout“. V oku by se už neměly o překot tvořit nové bílkovinné molekuly růstového faktoru VEGF, neměly by tu zběsile růst kapiláry a nemělo by docházet k poškození sítnice.
V první fázi klinických zkoušek bude pacientům podáván Cand5 přímo do nitra oka a lékaři budou sledovat, jestli to pacientům neškodí. Teprve v případě, že se neukážou nežádoucí vedlejší účinky, bude zahájena druhá fáze zkoušek, při nichž už půjde o posouzení léčebného efektu. Prozatím proběhly experimenty na opicích a ty naladily kapitány Acuity Pharmaceuticals na optimistickou notu. Zdá se, že buňky sítnice produkující VEGF podávanou siRNA přímo hltají.
„Jsou to takové popelnice,“ přiblížil chování těchto buněk vedoucí projektu Samuel Reich z Acuity Pharmaceuticals. „Skončí v nich každý cizí materiál, který se ocitne uvnitř oka.“
RNA interference není lidským vynálezem. Jako obvykle jsme ji „ošlehli“ z přírody. Je nastartována přítomností dvojšroubovicové molekuly RNA. Tento proces se zřejmě vyvinul jako ochranný mechanismus proti virům vybaveným dědičnou informací v podobě dvojité šroubovice RNA. Buňky se naučily ničit mRNA, která odpovídá pořadím písmen genetického kódu této dvojité šroubovici RNA a nadobro tak vypnou produkci bílkovin, která se podle této mRNA v buňce vyráběla. Je jasné, že tak je zabráněno viru v tom, aby si nechal buňkou vyrábět své bílkoviny. Jak už to v přírodě chodí, naučila se buňka mechanismu využít i pro jiné účely, např. pro regulaci genů. Taková vlastní dvojitá šroubovice RNA působí jako účinná brzda genu a přitom nepůsobí na úrovni DNA. Gen ať si klidně dělá co chce, RNA interference zabrání tomu, aby buňka pocítila důsledky „práce“ tohoto genu. Pokud bychom si dění v buňce rozdělili na tři patra: gen – RNA – bílkovina, pak RNA interference reguluje dění v buňce na úrovni „druhého patra“.
RNA interference se ukázala jako účinný „vypínač“ genů v mnoha pokusech, z nichž první proběhly na modelovém červu Caenorhabditis elegans koncem devadesátých let 20. století. Jasně se prokázalo, že dokáže úžasné kousky i v lidských buňkách. Nyní tedy aspiruje na praktické uplatnění.
Degenerace sítnice je vyvolána nadměrným růstem krevních kapilár, které mají křehké stěny, praskají a krev, která se z nich vylévá, pak ničí světločivné buňky. Za růst krevních kapilár může zvýšená produkce růstového faktoru VEGF. V Acuity Pharmaceuticals vyvinuli krátkou dvojšroubovici RNA (tzv. siRNA čili small interfering RNA – česky „malá interferující RNA“ ) označovanou kódem Cand5. Tato siRNA má pořadí „písmen“ genetického kódu shodnou s částí mRNA, podle které se v buňkách tvoří růstový faktor VEGF. Měla by proto zajistit rozložení mRNA pro VEGF a tím vlastně příslušný gen „vypnout“. V oku by se už neměly o překot tvořit nové bílkovinné molekuly růstového faktoru VEGF, neměly by tu zběsile růst kapiláry a nemělo by docházet k poškození sítnice.
V první fázi klinických zkoušek bude pacientům podáván Cand5 přímo do nitra oka a lékaři budou sledovat, jestli to pacientům neškodí. Teprve v případě, že se neukážou nežádoucí vedlejší účinky, bude zahájena druhá fáze zkoušek, při nichž už půjde o posouzení léčebného efektu. Prozatím proběhly experimenty na opicích a ty naladily kapitány Acuity Pharmaceuticals na optimistickou notu. Zdá se, že buňky sítnice produkující VEGF podávanou siRNA přímo hltají.
„Jsou to takové popelnice,“ přiblížil chování těchto buněk vedoucí projektu Samuel Reich z Acuity Pharmaceuticals. „Skončí v nich každý cizí materiál, který se ocitne uvnitř oka.“
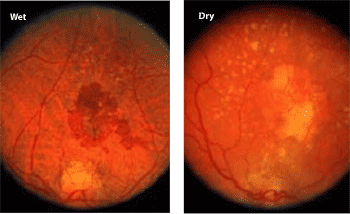
Degenerativní změny sítnice (tzv. AMD čili age-related macular degeneration) vyvolávající ztrátu zraku mají dvě formy – „mokrou“ (vlevo) a „suchou“. Při „suché“ AMD se na sítnici usazuje materiál, který je zplodinou metabolismu buněk sítnice a který je na snímku patrný jako světlejší skvrny. Tato forma AMD je mnohem častější, než „mokrá“ AMD, při které dochází k nadměrnému růstu krevních kapilár a krvácení, z jejich narušených stěn. Nový druh léčby pomocí siRNA je zaměřen na „mokrou“ AMD“.
Těm, kteří by si rádi udělali představu, jak funguje siRNA, doporučujeme vřele animovaný „film“ z webu časopisu Nature
Autor: Jaroslav Petr
Datum: 17.09.2004 00:55
Diskuze:



