
Kmenové buňky máme (my obratlovci) v těle až do vysokého věku. Jen jich je stále méně a méně. Ví se to již delší dobu. I to, že zvlášť markantní je jejich úbytek u syndromu předčasného stárnutí (progerie). S léčbou kmenovými buňkami je to ale jako na houpačce. Někdy dělají zázraky, jindy přivodí celou řadu komplikací. Často se špatně množí, a nebo se naopak množí dobře, ale zapomenou se diferencovat v to, co bychom od nich v poškozené tkáni potřebovali. U předčasného stárnutí zatím nebylo jasné, zda ztráta funkce těchto mladých buněk schopných nahrazovat ty opotřebované přispívá k procesu stárnutí a nebo zda je důsledkem procesu stárnutí. Výsledky pokusů na myších prováděných v Pennsylvanii nám na to nyní odpověd daly a léčbu stárnutí tak o velký kus přiblížily.
Máme konečně „věc Makropulos“?
Ne tak docela. Omlazení starých myšek má jeden háček. Johnny Huard z Pittsburgh School of Medicine a jeho kolegove z dalších pracovišť pokusničili na myškách s progerií. To nejsou obyčejné myši ale modelové organismy, které byly geneticky modifikovány, aby se jejich vývoj co nejvíce podobal nemoci, které se říká progerie. Jejich těla se super rychlé opotřebovávají. Myškám, stejně jako postiženým lidem se mnohem dříve vytrácí elasticita cév, zužují se a to vede k předčasné ateroskleróze. Kosterním svalům se nedostává živin, dostavují se křeče a svalová hmota se ztrácí. Také srdeční sval nemá dostatečný přísun kyslíku a vyvíjí se angína pectoris s typickými bolestmi na hrudi. Srdce následkem nedostatečného zásobení krví trpí infarkty a selhává. Ke společným, rychle postupujícím neduhům vyššího věku se přidává stařecký třes, ztráta koordinace pohybu. Myšky se nedožívají ani měsíce a hynou mezi 21. až 28. dnem po narození.
Když těmto předčasně stárnoucím zvířátkům vědci v jejich kmetském věku (ten je pro ně pouhých 17 dnů) vstříkli do těla kmenové buňky získané od zdravých mladých myšek, evidentně jim to prospělo, problémy postupujícího stáří se nedostavily, nebo až mnohem později. Ve zdraví se dožívaly dvou měsíců a déle.
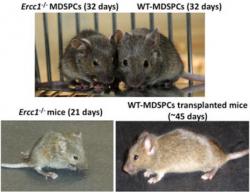
To nejdůležitější na pokusech se zvířecím stárnutím ale je, že daly odpověď na otázku co je příčinou změn, které doprovázejí předčasné stárnutí. Nyní víme, že to je špatná funkce kmenových buněk (nebo buněk jim hodně podobných). Vyplynulo to z kontrolních pokusů, při nichž injekce kmenovými buňkami získanými z mladých, ale progerií trpících myšek, léčebný efekt u pacientek nenavodily. Stejně tak dopadl pokus s aplikací kmenových buněk získaných od zdravých, ale velmi starých myší. Taková léčba nemocné hlodavce od aterosklerózy, osteoartrózy, osteoporózy a dalších radostí stáří také neochránila.
Půjde to využít i u lidi?
U pacientů trpících syndromem předčasného stárnutí s vysokou pravděpodobností ano. Jen taková léčba narazí na etický problém - kde sehnat dostatek kvalitních kmenových buněk bez toho, aby se použily potracené lidské plody, nebo nechtěná embrya čekající v tekutém dusíku na likvidaci. Pokud by se ale takové buňky podařilo připravit jinou cestou, ověřovacím klinickým pokusům by nemělo stát nic v cestě a mohlo by zřejmě přijít velmi rychle na přetřes i prodlužování aktivního způsobu života těm, kteří progerií netrpí, ale své tkáně si opotřebovali z nějakého jiného důvodu také rychleji, než je zdrávo. Na to, že se toto "omlazování" objeví v nabídkových katalozích transplantační turistiky dříve, než ji u nás stačíme ověřit, na to si můžeme vsadit již nyní.
Možná to později půjde i bez buněk
Bližší vyšetření léčených myšek totiž ukázalo, že ke zlepšení krevního zásobení svalů a mozku došlo i v místech, kam se omlazovací buňky ani nedostaly. K léčbě jejich mozků a ochablých končetin na něž by jim za pár dnů dělalo problém se i jen postavit, postačovalo vstřiknout jim před úplným zhoršením zdravotního stavu kmenové buňky do břicha. I když z dutiny břišní nijak zvlášť necestovaly, rozhodně ne až do mozku, dosáhly svým léčebným efektem i tam. Jejich „dlouhými prsty“ je asi nějaká zatím nám neznámá substance, která v okolních tkáních vytváří prostředí, jenž je pak do určité míry schopné poškozeným a nemocným buňkám zlepšovat jejich stav a korigovat tak různé orgánové dysfunkce. Možná se brzo dočkáme toho, že americkým vědcům se podaří zjistit, co vlastně injikované buňky produkují a co se za jejich omlazovacím efektem ukrývá. Mohou to být jak proteiny, tak i nějaké jiné molekuly. A právě v tom by mohlo být největší kouzlo budoucího omlazování. Zatimco léčba kmenovými buňkami se ráda zvrhne v rakovinu, léčba pomocí proteinů, peptidů či jiných molekul, by takovou necnost mít neměla. A také tu je naděje, že účinné substance půjde vyrábět snadno a levně...
Pramen: University of Pittsburgh Schools of the Health Sciences
Diskuze:



