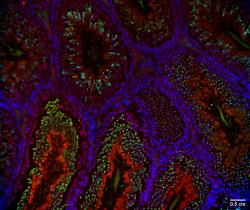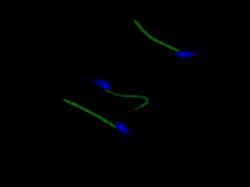
Těžko bychom hledali v lidském organizmu buňky, které jsou odlišnější než spermie a vajíčko. Snad i proto se mohou vyvíjet jen samostatně a jedinec by nesnesl břemeno vývoje obou těchto protipólů – Marsu i Venuše, v jedné tělesné schránce. Přesto však mají obě gamety leccos společného: poloviční porci genetické informace, splynutím dávají vzniknout zygotě a novému životu, vyvíjí se v pohlavních žlázách a jejich zrání a použití je nesmlouvavě podmíněno pohlavní dospělostí nebo alespoň pubertou, sexuálním apetitem a možností potkat se se svým vhodným protějškem v čase a prostoru. Je tu ale ještě jedna společná vlastnost, která často uniká naší pozornosti a někdy i chápání: spermie i vajíčka jsou transkripčně inaktivní! Co to znamená? Nemohou manifestovat svůj genom, nemohou syntetizovat proteiny; jsou odkázané na aparát somatických buněk, které jim umožní dozrát a které je, když to alespoň trochu jde, doprovází co nejdále na jejich pouti k oplození. Když se ale pohlavní buňky osamostatní, jsou odkázány samy na sebe. Zatímco vajíčko je na běžné poměry obrovskou buňkou se schopností akumulovat potřebné molekuly, proteiny a organely v dostatečném množství, spermie jsou na tom o poznání hůře: jsou malé, nedisponují žádnými depozity pro proteiny, navíc jsou pohyblivé a náročné na energii, musí mezi sebou soutěžit a tak na růžích rozhodně ustláno nemají. Aby toho nebylo málo, nachází se v minutě pravdy, tedy po ejakulaci na cestě k vytouženému vajíčku, ve velmi náročném prostředí, které lze bez nadsázky přirovnat k maratonu. Co víc! Po tomto výkonu teprve vše začíná, protože až v horní části vejcovodu dochází ke kýženému oplození.
Není divu, že evoluce byla k spermiím nevybíravá. Výsledkem je skutečnost, že proteinová výbava spermie musí být ochráněna, jak jen to jde, aby byla co k čemu, až bude zapotřebí: pohyb bičíku po ejakulaci, ztřeštěný pohyb bičíku po kapacitaci, receptory připravené pro chemotaxi vyvolanou ovulovaným vajíčkem, enzymatická hydrolýza extracelulární matrix buněk doprovázející vajíčko, penetrace skrz glykoproteinový obal vajíčka (zona pellucida), vazba na membránu vajíčka, ale také schopnost přesvědčit vajíčko k embryonálnímu vývoji. Dobrá spermie tak musí zvládnout hodně nástrah na to, abychom jí mohli s nadsázkou považovat za všeho schopného „Ferdu mravence“. A v čem spočívá kouzlo dobré spermie? Jsou to post-translační modifikace jejich proteinů.
Zatímco somatické buňky celého našeho těla žijí v luxusu homeostázy (stálosti vnitřního prostředí) a mohou si ze svého genomu syntetizovat kdykoliv cokoliv a v jakémkoliv množství, spermie jsou na tom jinak: mají v ranečku zabaleno na cestu a proteiny, které potřebují později, musí chránit. Modifikace těchto proteinů na různých aminokyselinách jim v tom pomáhají anebo proteiny naopak stimulují k aktivitě – fosforylace threoninu, fosforylace serinu, acetylace lysinu, ubiquitinace lysinu, atd. Významným stabilizátorem proteinů jsou disulfidické můstky mezi cysteiny. Jakmile disulfidické můstky padnou, zmocní se cysteinů vysoce reaktivní volné radikály a přemění je na nitrosocystein či sulfenovou kyselinu. Takový protein má našlápnuto k degradaci a s ním i celá spermie. A přitom je redukce disulfidických můstků nutná pro aktivitu řady proteinů, jak tohle vyřešit? Pro redukované disulfidické můstky je tu ale naděje – sirovodík! Ano, tento jedovatý plyn, dnes správněji nazývaný sulfan, je ve velmi malém množství buňkami přirozeně uvolňován s cílem modifikovat cysteiny a vytvořit jedinečnou proteinovou modifikaci – sulfhydrataci. Jakmile byla tato modifikace popsána na somatických buňkách, stala se částečně objasněním a z části velikou výzvou pro reprodukční biologii: vždyť máme vysvětlení pro přirozenou ochranu proteinů před degradací po rozpuštění disulfidických můstků! Pokud má buňka přirozenou ochranu před degradací proteinů, můžeme si jí ochočit v laboratorních podmínkách a pomoci mužům trpící neplodností? To jsou otázky, které dávají základ pro postulát, hypotézu, stanovený cíl a roky práce v laboratoři. Výsledkem je objev sulfanu ve spermii, jeho přirozená produkce ve varleti, přítomnost ve spermii, schopnost modifikovat proteiny spermie a tak i její klíčové vlastnosti, které z ní činí naději na nový život.
Přestože lék na mužskou neplodnost na sebe nechá ještě nějaký čas čekat, bez základních poznatků se neobejde. Naštěstí byl základní kámen takového poznání položen – ve spermiích je řada klíčových proteinů, které jsou modifikovány sirovodíkem, resp. sulfhydratací. A nejsou to proteiny ledajaké – odpovídají za ustanovení dalších modifikací (fosforylace) a tedy aktivity celé mašinérie dalších proteinů spermie, proteiny řídící pohyb spermie, její integritu, životaschopnost a zejména schopnost oplození. Nejnovější poznatky nás přesvědčují, že spermie bez sulfanu nemá šanci a právě sulfan z ní dělá favorita pro oplození. Pro diagnostiku a léčbu neplodnosti se tak po čase snad blýská na lepší časy.
Poznámka: Více na: https://pubmed.ncbi.nlm.nih.gov/35794129/
Diskuze: